题目内容
【题目】将0.2mol两种气态烃组成的混合气完全燃烧后得到6.72L二氧化碳(标准状况下)和7.2g水,下列关于该混合烃说法正确的是( )
A.一定有乙烯B.一定有甲烷
C.一定是甲烷和乙烯的混合气体D.可能有乙炔
【答案】B
【解析】
根据![]() 计算水的物质的量,根据
计算水的物质的量,根据![]() 计算二氧化碳的物质的量,根据H原子、C原子守恒计算混合物的平均分子组成,据此判断。
计算二氧化碳的物质的量,根据H原子、C原子守恒计算混合物的平均分子组成,据此判断。
两种气态烃组成的混合物0.2mol完全燃烧得6.72L二氧化碳和7.2克水,7.2克水的物质的量为![]() =0.4mol,平均分子组成中H原子数目为:
=0.4mol,平均分子组成中H原子数目为:![]() ,6.72L二氧化碳的物质的量=
,6.72L二氧化碳的物质的量=![]() =0.3mol,平均分子组成C原子数目为:
=0.3mol,平均分子组成C原子数目为:![]() ,故该混合烃的平均分子式为C1.5H4,根据C原子可知,该烃一定含有CH4,根据H原子可知,另一烃的分子中H原子数目为4,故ACD错误、B正确。
,故该混合烃的平均分子式为C1.5H4,根据C原子可知,该烃一定含有CH4,根据H原子可知,另一烃的分子中H原子数目为4,故ACD错误、B正确。
答案选B。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
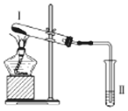
【题目】按如图装置进行实验,下列推断正确的是( )
选项 | I中试剂 | II中试剂及现象 | 推断 | |
A | 铁粉与湿棉花 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
|
B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 | |
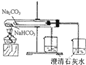
C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油分解产物中含有不饱和烃 | |
D | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
A.AB.BC.CD.D
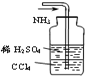
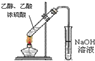
【题目】利用右图所示装置进行下列实验,其中丙中实验现象描述正确的是
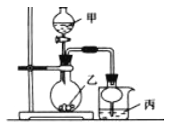
实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
A | 70%硫酸 | Na2SO3 | 紫色石蕊试液 | 溶液先变红后褪色 |
B | 浓盐酸 | KMnO4 | 含酚酞的NaOH溶液 | 溶液褪色 |
C | 稀盐酸 | CaCO3 | BaCI2溶液 | 有白色沉淀生成 |
D | 浓氨水 | CaO | AlCl3 | 先生成白色沉淀然后沉淀溶解 |
A. A B. B C. C D. D