题目内容
【题目】某小组利用如下装置制备Cu(NH3)xSO4·H2O(溶于水呈深蓝色).并测量x值。

(Cu(NH3)xSO4·H2O制备)见图1
(1)A中发生的化学反应方程式为_____________________________ 。
(2)B中观察到的现象是_______________________;C中CCl4的作用是 ______________。
(3)欲从Cu(NH3)xSO4溶液中析出Cu(NH3)xSO4·H2O晶体,可加入试剂 _______________ 。
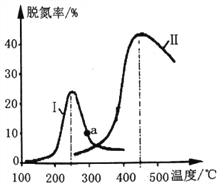
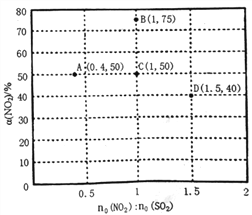
(x值的测量)见图2
步骤一:检查装置气密性,称取0.4690g晶体[M = (178+17x)g/mol]于锥形瓶a中;
步骤二:通过分液漏斗向锥形瓶a中滴加l0%NaOH溶液;
步骤三:用0. 5000 mol/L的NaOH标液滴定b中剩余HCI,消耗标液16. 00 mL。
(4)步骤二的反应可理解为Cu(NH3)xSO4与NaOH在溶液中反应,其离子方程式为 ______。
(x值的计算与论证)
(5)计算:x = __________ ,
该学习小组针对上述实验步骤,提出测量值(x)比理论值偏小的原因如下:
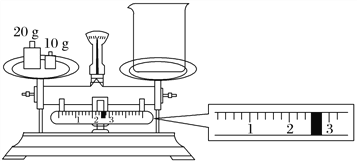
假设1:步骤一中用于称量的天平砝码腐蚀缺损;
假设2:步骤二中 _______________________________________________(任写两点);
假设3 :步骤三中测定结束读数时,体积读数偏小。该假设_____(填“成立”或“不成立”)。
(6)针对假设l,你对实验的处理意见是________________。
【答案】Ca(OH)2+2NH4Cl=△2NH3↑+CaCl2+2H2O由蓝色溶液变为蓝色沉淀,随后沉淀溶解变成深蓝色溶液防止倒吸无水乙醇Cu(NH3)x2++2OH—= Cu(OH)2↓+xNH3↑3.56加入NaOH溶液不足,没有加热或生成氨气未完全溢出等不成立更换砝码完好的托盘天平后,重新进行步骤一到三的全部实验
【解析】
试题(1)A为实验室制取氨气的装置,是利用氯化铵与氢氧化钙固体加热,反应的化学方程式是2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;氨气通入硫酸铜溶液中,开始生成氢氧化铜蓝色沉淀,随着氨气的通入,则氨气与氢氧化铜反应生成四氨合铜离子,后沉淀逐渐溶解,转化为深蓝色溶液;
2NH3↑+CaCl2+2H2O;氨气通入硫酸铜溶液中,开始生成氢氧化铜蓝色沉淀,随着氨气的通入,则氨气与氢氧化铜反应生成四氨合铜离子,后沉淀逐渐溶解,转化为深蓝色溶液;
(2)四氯化碳的密度大于水,因为氨气直接通入水中,会发生倒吸现象,氨气不溶于四氯化碳,通过四氯化碳的缓冲作用,可以防止发生倒吸;
(3)欲从Cu(NH3)xSO4溶液中析出Cu(NH3)xSO4·H2O晶体,可加入试剂无水乙醇,因为乙醇的极性较小,且该晶体在乙醇中的溶解度小于在水中的溶解度,有利于晶体的析出;
(4)Cu(NH3)xSO4与NaOH在溶液中反应,生成硫酸钠、氢氧化铜和氨气,所以反应的离子方程式为Cu(NH3)x2++2OH-= Cu(OH)2↓+xNH3↑;
(5)b中原来HCl的物质的量是0.03L×0.5000mol/L=0.015mol,剩余HCl的物质的量是0.016L×0.5000mol/L=0.008mol,则与氨气反应的HCl的物质的量也是氨气的物质的量是0.015-0.008=0.007mol;则0.4690g/(178+17x)g/mol×x=0.007mol,解得x=3.56;测定结果偏小,可能步骤二加入NaOH溶液不足,没有加热或生成的氨气未完全逸出等;
步骤三中测定结束读数时,体积读数偏小,则说明剩余HCl偏小,则与氨气反应的HCl偏多,则氨气的物质的量偏大,测定结果应偏高,所以不成立;
针对假设l,可更换砝码完好的天平后重新进行步骤一到步骤三全部实验,再进行测定。