题目内容
11.不能用H++OH-=H2O来表示的化学反应是( )| A. | NaOH溶液与盐酸反应 | B. | KOH溶液与稀硫酸反应 | ||
| C. | Ba(OH)2溶液与稀硫酸反应 | D. | 澄清石灰水与稀硝酸反应 |
分析 离子方程式H++OH-=H2O表示强酸和强碱反应生成可溶性的盐和水的一类反应,据此进行判断.
解答 解:A.NaOH溶液与盐酸反应的离子方程式为:H++OH-=H2O,不符合条件,故A错误;
B.KOH溶液与稀硫酸反应的离子方程式为:H++OH-=H2O,不符合条件,故B错误
C.Ba(OH)2溶液与稀硫酸反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用离子方程式H++OH-=H2O表示,符合条件,故C正确;
D.澄清石灰水与稀硝酸反应的离子方程式为:H++OH-=H2O,不符合条件,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,如:各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列物质中属于电解质,且能导电的是( )
| A. | 熔融的氢氧化钾 | B. | 液态铜 | C. | 液态氯化氢 | D. | 固态氯化钾 |
2.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 向饱和碳酸钠溶液中通入CO2 | 有晶体析出 | 溶解度:NaHCO3>Na2CO3 |
| D | 向盛有少量NaHCO3的试管中滴加草酸溶液 | 有气泡产生 | 酸性:草酸>碳酸 |
| A. | A | B. | B | C. | C | D. | D |
16.2011年3月11日的日本大地震造成日本福岛核电站出现严重事故,由核反应堆泄漏出的${\;}_{53}^{131}$I和罗${\;}_{55}^{137}$Cs引起了全世界的关注,其中${\;}_{55}^{137}$Cs原子核内的中子数为( )
| A. | 82 | B. | 55 | C. | 137 | D. | 192 |
3.室温下,将 0.1mol下列物质置于1L 水中充分搅拌后,溶液中阴离子数最多的是( )
| A. | KC1 | B. | MgCl2 | C. | Na2CO3 | D. | K2SO4 |
20.下列实验操作中正确的是( )
| A. | 分液时,先从分液漏斗下口放出下层液体,更换烧杯后再从下口放出上层液体 | |
| B. | 蒸馏时,温度计水银球需靠近蒸馏烧瓶支管口,冷凝水的流向需从冷凝管的上进水口流入,下进水口流出 | |
| C. | 分离硝酸钾与氯化钾时,冷却结晶时析出的是溶解度随温度变化较大的固体 | |
| D. | 用托盘天平称量10.2 g固体时,如果砝码误放于左盘,固体放在右盘,则实际称得的固体质量大于10.2 g |
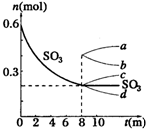 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g);△H>0,其中SO3的变化如图所示:
在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g);△H>0,其中SO3的变化如图所示: