��Ŀ����
����Ŀ����֪�װ�(CN3NH2)��һ�ּ��Ա�һˮ�ϰ�ǿ��һԪ��������£��������Ϊ100mL��cmol/L�װ���Һ0.1mol/LNaOH��Һ�зֱ�ͨ��HCl���塣lg ��ͨ������ʵ����ı仯��ͼ��ʾ(��������Һ����ı仯)�������й�˵���������( )
��ͨ������ʵ����ı仯��ͼ��ʾ(��������Һ����ı仯)�������й�˵���������( )

A.����MOH��������������Һ�ı仯����
B.��a��b��c�����У�c���Ӧ��Һ��ˮ�ĵ���̶����
C.�����£���ˮϡ��b����Һ����Һ����������Ũ�ȶ���С
D.c���Ӧ����Һ�У�c(Cl-)=c(CH3NH3+)��c(H+)=c(OH-)
���𰸡�C
��������
�����£�0.1mol/LNaOH��Һ�У�c(OH-)=0.1mol/L��Kw=10-14����c(H+)=10-13mol/L��lg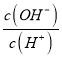 =12��MOH������ΪNaOH����ROHΪCN3NH2��
=12��MOH������ΪNaOH����ROHΪCN3NH2��
A��������֪������MOH����NaOH��Һ�ı仯���ߣ�A˵����ȷ��
B����a��b��c�����У�a��ΪNaOH��Һ��������ǿ������ˮ�ĵ���̶����b��c(OH-)=10-4mol/L��ΪCN3NH2��CN3NH3Cl�Ļ��Һ������ˮ�ĵ�����c��c(H+)= c(OH-)����ˮ�ĵ������Ƴ̶ȼ�������c���Ӧ��Һ��ˮ�ĵ���̶����B˵����ȷ��
C�������£�b��ΪCN3NH2��CN3NH3Cl�Ļ��Һ����Һ�ʼ��ԣ���ˮϡ��b����Һ����Һ��c(OH-)��С���¶Ȳ��䣬��Kw���䣬c(H+)����C˵������
D��c��c(H+)=c(OH-)=10-7mol/L�����ݵ���غ㣬c(CH3NH3+)+c(H+)=c(Cl-)+c(OH-)����c(CH3NH3+)=c(Cl-)����ԶԶ����c(H+)���ʶ�Ӧ����Һ�У�c(Cl-)=c(CH3NH3+)��c(H+)=c(OH-)��D˵����ȷ��
��ΪC��

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�