题目内容
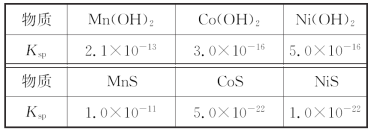
【题目】锰是冶炼工业中常用的添加剂。以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下,已知25℃,部分物质的溶度积常数如下:
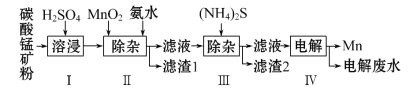
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是______________。
(2)步骤Ⅱ中,MnO2在酸性条件下将Fe2+氧化为Fe3+,反应的离子方程式是__________________,加氨水调节溶液的pH为5.0~6.0,以除去Fe3+。
(3)步骤Ⅲ中,滤渣2的主要成分是________。
(4)步骤Ⅳ中,在________(填“阴”或“阳”)极析出Mn,电极反应为___________________。
【答案】
(1)MnCO3+H2SO4=MnSO4+CO2↑+H2O
(2)MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O
(3)CoS和NiS
(4)阴;Mn2++2e-=Mn
【解析】
试题分析:(1)碳酸锰与硫酸反应生成硫酸锰、二氧化碳和水,化学方程式为MnCO3+H2SO4=MnSO4+CO2↑+H2O,故答案为:MnCO3+H2SO4=MnSO4+CO2↑+H2O;
(2)MnO2在酸性条件下可将Fe2+氧化为Fe3+,MnO2被还原成Mn2+,发生反应的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(3)步骤Ⅲ中加入(NH4)2S,除掉的是Co2+和Ni2+,所以滤渣2的主要成分是CoS和NiS,故答案为:CoS和NiS;
(4)Mn2+在阴极发生还原反应生成Mn,电极反应为Mn2++2e-=Mn,故答案为:阴;Mn2++2e-=Mn。

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目