题目内容
(10)(1)(6分)2mol CO2中含______ mol碳原子__________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L,质量是______________g。1 mol·L-1的CaCl2 溶液0.5L,Cl- 离子的物质的量浓度为___________、Ca2+物质的量为 。
(2))(4分)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③水银 ④蔗糖 ⑤醋酸 ⑥KNO3溶液 ⑦氨气 ⑧碳酸钙 ⑨二氧化硫 填空回答(填序号):
(1)以上物质中属于强电解质的是 ;
(2)以上物质中属于非电解质的是 ;
(16分)(12分)(1)2, 4 NA ,44.8 , 88 . 2 mol·L-1, 0.5mol
(4分)(2)①②(8) ;(2)④(7 )(9);

练习册系列答案
相关题目
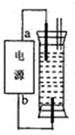 (2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:
(2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程: 在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.
在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡.