题目内容
下列实验操作错误的是( )
| A、要分离氯化钾、二氧化锰的混合物可通过溶解、过滤、蒸发等操作来完成 |
| B、检验某溶液中是否含SO42-时,应向该溶液中依次加入BaCl2溶液和稀盐酸 |
| C、向含FeSO4杂质的MgSO4溶液中依次加入过氧化氢、碳酸镁,充分搅拌后过滤,可除去FeSO4杂质,得到较纯净的MgSO4溶液 |
| D、测定硫酸铜晶体中结晶水含量时,要灼烧至固体完全变白 |
考点:化学实验方案的评价,物质的分离、提纯和除杂,物质的检验和鉴别的基本方法选择及应用
专题:实验评价题
分析:A.氯化钾溶于水,二氧化锰不溶;
B.应先加入盐酸,再加氯化钡;
C.加入过氧化氢,可氧化亚铁离子生成铁离子,加入碳酸镁起到调节溶液pH的作用;
D.灼烧至固体完全变白,可完全失去结晶水.
B.应先加入盐酸,再加氯化钡;
C.加入过氧化氢,可氧化亚铁离子生成铁离子,加入碳酸镁起到调节溶液pH的作用;
D.灼烧至固体完全变白,可完全失去结晶水.
解答:
解:A.氯化钾溶于水,二氧化锰不溶,可加水溶解氯化钾,过滤分离二氧化锰,然后蒸发、结晶可得到氯化钾,故A正确;
B.应先加入盐酸,如无现象,再加氯化钡,如生成沉淀,可说明含有硫酸根离子,故B错误;
C.加入过氧化氢,可氧化亚铁离子生成铁离子,加入碳酸镁起到调节溶液pH的作用,促使铁离子水解生成沉淀而除去,且没有引入新杂质,故C正确;
D.灼烧至固体完全变白,可完全失去结晶水,避免误差,故D正确.
故选B.
B.应先加入盐酸,如无现象,再加氯化钡,如生成沉淀,可说明含有硫酸根离子,故B错误;
C.加入过氧化氢,可氧化亚铁离子生成铁离子,加入碳酸镁起到调节溶液pH的作用,促使铁离子水解生成沉淀而除去,且没有引入新杂质,故C正确;
D.灼烧至固体完全变白,可完全失去结晶水,避免误差,故D正确.
故选B.
点评:本题考查较为综合,涉及物质的检验、分离等操作,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于苯的说法中,不正确的是( )
| A、分子中含有三个C-C键和三个C=C键 |
| B、在空气中燃烧时产生较多的黑烟 |
| C、分子中C、H元素的质量为12:1 |
| D、在一定条件下可与氢气发生加成反应 |
室温下向一定量的稀氨水中加入水稀释后,下列说法正确的是( )
| A、因为稀释,溶液中所有离子的浓度均减小 | ||
B、溶液中
| ||
| C、NH3?H2O的电离程度增大,c(OH-)亦增大 | ||
| D、再加入与氨水等体积等浓度的盐酸,混合液pH=7 |
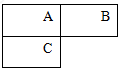 A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )
A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )①B、C形成的单质均存在同素异形体
②X的种类比Y多
③常温下,B的氢化物不能电离出H+
④C的最高价氧化物对应的水化物是强酸.
| A、①②③④ | B、②④ |
| C、①② | D、①③ |
门捷列夫制作元素周期表时,许多元素尚未发现,他在铝的下面留了空位给“类铝”,并对“类铝”的性质进行了预测,“类铝”与后来发现的镓的性质一致,从而验证了元素周期表的正确性.下列有关镓的性质的描述中错误的是( )
| A、镓的金属性比铝弱 |
| B、镓的常见化合价为+3 |
| C、镓的原子半径比铝大 |
| D、镓的单质有导电性 |
在氯化铁和盐酸的混合溶液中,已知c(Cl-)═a mol/L,pH═b<1,则溶液中c(Fe3+)为( )
A、
| ||
| B、(a-1×10-b) mol/L | ||
C、(a-
| ||
| D、上述答案都不正确 |
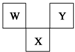 如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )
如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )| A、三种元素的原子半径的大小顺序是W<Y<X |
| B、X元素的氧化物、氢化物的水溶液都呈酸性 |
| C、Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质 |
| D、W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性 |