题目内容
下列标有横线的物质在给定的条件下不能完全溶解的是( )
①1mol Zn与含1mol H2SO4的稀硫酸溶液反应 ②1mol Cu与含2mol H2SO4的浓硫酸溶液共热
③1mol Cu与含4mol HNO3的浓硝酸溶液反应 ④1mol MnO2与含4mol HCl的浓盐酸溶液共热.
①1mol Zn与含1mol H2SO4的稀硫酸溶液反应 ②1mol Cu与含2mol H2SO4的浓硫酸溶液共热
③1mol Cu与含4mol HNO3的浓硝酸溶液反应 ④1mol MnO2与含4mol HCl的浓盐酸溶液共热.
| A、①③ | B、①② | C、②④ | D、③④ |
考点:硝酸的化学性质,氯、溴、碘及其化合物的综合应用,浓硫酸的性质
专题:元素及其化合物
分析:①1mol锌与含1mol H2SO4的稀硫酸溶液恰好完全反应;
②随反应的进行浓硫酸变在稀硫酸,稀硫酸与铜不反应;
③1mol铜转移2mol的电子,生成2mol的铜离子与2mol硝酸结合成硫酸盐,而2mol HNO3的硝酸作氧化剂,得电子的量为2mol~6mol,所以铜不足;
④稀盐酸与二氧化锰不反应.
②随反应的进行浓硫酸变在稀硫酸,稀硫酸与铜不反应;
③1mol铜转移2mol的电子,生成2mol的铜离子与2mol硝酸结合成硫酸盐,而2mol HNO3的硝酸作氧化剂,得电子的量为2mol~6mol,所以铜不足;
④稀盐酸与二氧化锰不反应.
解答:
解:①1mol锌与含1mol H2SO4的稀硫酸溶液恰好完全反应,故不选;
②随反应的进行浓硫酸变在稀硫酸,稀硫酸与铜不反应,故选;
③1mol铜转移2mol的电子,生成2mol的铜离子与2mol硝酸结合成硫酸盐,而2mol HNO3的硝酸作氧化剂,得电子的量为2mol~6mol,所以铜不足,故不选;
④随着反应的进行,盐酸浓度逐渐降低,稀盐酸与二氧化锰不反应,故选.
故选C.
②随反应的进行浓硫酸变在稀硫酸,稀硫酸与铜不反应,故选;
③1mol铜转移2mol的电子,生成2mol的铜离子与2mol硝酸结合成硫酸盐,而2mol HNO3的硝酸作氧化剂,得电子的量为2mol~6mol,所以铜不足,故不选;
④随着反应的进行,盐酸浓度逐渐降低,稀盐酸与二氧化锰不反应,故选.
故选C.
点评:本题综合考查元素化合物知识,涉及浓硫酸、硝酸、氯气的制备等,综合考查元素化合物知识的运用,为高频常见题型,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
下列说法中正确的一组是( )
| A、正丁烷和异丁烷是同系物 |
| B、CH3CH2CH2CH(C2H5)CH3和C2H5CH(CH3)CH2CH2CH3是同一种物质 |
| C、H2和D2互为同位素 |
D、 和 和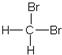 互为同分异构体 互为同分异构体 |
下列有关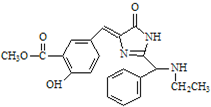 的说法中不正确的是( )
的说法中不正确的是( )
 的说法中不正确的是( )
的说法中不正确的是( )| A、该有机物能发生水解反应 |
| B、该有机物的化学式为C21H20N3O4 |
| C、该有机物不能发生消去反应 |
| D、该有机物既能与溴水反应,又能与碳酸钠溶液反应 |
以下物质保存方法不正确的是( )
| A、浓硝酸保存在棕色试剂瓶中 |
| B、氢氧化钠溶液保存在配有玻璃塞的细口瓶中 |
| C、少量金属钠保存在煤油中 |
| D、少量白磷保存在水中 |
实验室为了妥善保存硫酸亚铁溶液,常加入少量的( )
| A、锌粉 | B、铜粉 | C、铁粉 | D、镁粉 |
设NA代表阿伏伽德罗常数的值,下列说法中正确的是( )
| A、NA个氯气分子与NA氢气分子的质量比等于35.5:1 |
| B、在常温常压下,11.2L氯气含有分子数为0.5NA |
| C、与7.8g Na2O2完全反应时,消耗H2O的分子数为0.2NA |
| D、1L 0.5mol?L-1硝酸钡溶液中所含NO3-数为0.5NA |
铍元素性质与铝元素性质相似,下列方法能证明氯化铍由共价键构成的是( )
| A、溶于水加硝酸银溶液,观察是否有白色沉淀生成 |
| B、溶于水做导电实验,观察是否导电 |
| C、熔融状态,做导电实验,观察是否导电 |
| D、测定氯化铍熔点 |
由乙醇为主要原料制取乙二醇,需要经过的反应为( )
| A、取代-水解 |
| B、取代-消去-加成 |
| C、消去-加成 |
| D、消去-加成-水解 |
只用水不能鉴别的一组物质是( )
| A、酒精和乙酸 |
| B、苯和酒精 |
| C、苯和四氯化碳 |
| D、硝基苯和溴苯 |