题目内容
某厂废水中含5.00×2013-3mol·L-1的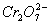 ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料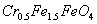 (
(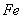 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:
(1)第①步反应的离子方程式是
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有
(4)欲使1L该废水中的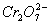 完全转化为
完全转化为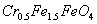 。理论上需要加入
。理论上需要加入
GFeSO4·7H2O。
【答案】
(1)Cr2O72- + 6Fe2+ + 14H+  2Cr3+ + 6Fe3+ + 7H2O
2Cr3+ + 6Fe3+ + 7H2O
(2)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照。
(3)Fe(OH)3、Fe(OH)2
(4)13.9
【解析】(1)第①步是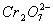 与Fe2+发生氧化还原反应,方程式为:
与Fe2+发生氧化还原反应,方程式为: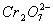 +6Fe2++14H+=2Cr3++6Fe3++7H2O;
+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(2)测定溶液的pH的方法是:用玻璃棒蘸取待测溶液滴在pH试纸的中心位置,然后对照标准比色卡,读出对应颜色的数据;
(3)从最终所得磁性材料的化学式可知,滤渣中主要有Cr(OH)3、Fe(OH)2、Fe(OH)3;
(4)1L废水中的n(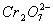 )=5.00×2013-3mol,根据关系式:
)=5.00×2013-3mol,根据关系式: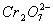 ~4Cr0.5Fe1.5FeO4~2013FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol×278g·mol-1=13.9g。
~4Cr0.5Fe1.5FeO4~2013FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol×278g·mol-1=13.9g。
【考点分析】根据新信息书写离子方程式,及其离子反应的综合运用。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、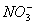 、SO
、SO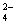 、
、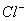 、
、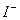 、
、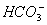 ,取该溶液实验如下:
,取该溶液实验如下:
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| ②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,后在空气中又变成红棕色 |
| ③取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ⑤取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(1)溶液中肯定存在的离子是________________________。
(2)溶液中肯定不存在的离子是________________________。
(3)为进一步确定其他离子,应该补充的实验是________ _ ________
。
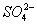 、Fe3+
、Fe3+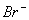
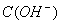 =1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( )
=1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( ) 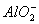 D. K+ 、 NH4+、
D. K+ 、 NH4+、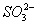 、
、 H++CH3COO-,下列叙述不正确的是 ( )
H++CH3COO-,下列叙述不正确的是 ( )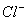 )>C(
)>C(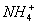 )>C(H+)>C(
)>C(H+)>C(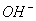 )
)