题目内容
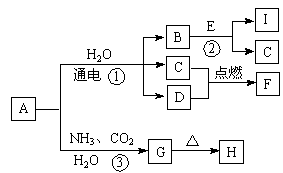
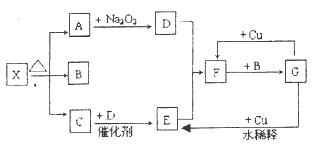
A、B、C、D、E、F、X存在如图所示转换关系,其中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。X可能是强酸,也可能是强碱。
(1)A的化学式是___________________。
(2)若X是强酸,将D与Cl2同时通入水中发生反应的离子方程式为_____________________________。
(3)若X是强碱,过量的B跟Cl2反应除生成C外,另一产物是氯化物。
①过量的B跟Cl2反应的化学方程式为______________________。
②工业生产中B→D的化学方程式为_______________________。
(1)(NH4)2S(2分) (2)Cl2+SO2+2H2O=4H++SO42-+2Cl-(2分)
(3)①3Cl2+8NH3=N2+6NH4Cl(2分) ②4NH3+5O2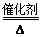 4NO+6H2O(2分)
4NO+6H2O(2分)
解析试题分析:(1)正盐A既能和强酸反应生成氢化物,也能喝强碱反应生成氢化物,则A一定是弱酸的铵盐。E能和水反应生成强酸F,因此E是NO2或三氧化硫。则A是硫化铵,化学式为(NH4)2S。
(2)若X是强酸,则B是H2S。H2S被氯气氧化生成单质硫,即C是S。所以D是SO2,E是三氧化硫,F是硫酸。氯气具有氧化性,能把SO2氧化生成硫酸,所以将D与Cl2同时通入水中发生反应的离子方程式为Cl2+SO2+2H2O=4H++SO42-+2Cl-。
(3)若X是强碱,则B是氨气。氨气被氯气氧化生成氮气,所以C是氮气。则D是NO,E是NO2。
①氯气氧化氨气生成氮气和氯化氢,过量的氨气跟氯化氢反应生成氯化铵,因此过量的B跟Cl2反应的化学方程式为3Cl2+8NH3=N2+6NH4Cl。
②工业生产中B→D所以氨的催化氧化,反应的化学方程式为4NH3+5O2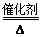 4NO+6H2O。
4NO+6H2O。
考点:考查氮、硫及其化合物转化的有关判断

 阅读快车系列答案
阅读快车系列答案