题目内容
3.25℃时,pH=12的Ba(OH)2溶液中,由水电离出的OH-浓度是( )| A. | 2×10-2mol•L-1 | B. | 1×10-12mol•L-1 | C. | 1×10-2mol•L-1 | D. | 2×10-12mol•L-1. |
分析 pH=12的Ba(OH)2溶液中,氢氧根离子抑制了水的电离,溶液中氢离子都是由水电离产生,水电离产生的c(H+)等于溶液中水电离出c(OH-),检测进行计算.
解答 解:pH=12的Ba(OH)2溶液中氢离子由水电离产生,水电离产生的c(H+)等于溶液中水电离出c(OH-),
故水电离出氢氧根离子浓度为:c(OH-)=c(H+)=10-12mol/L,
故选B.
点评 本题考查了溶液pH的计算、水的电离及其影响,题目难度中等,明确碱溶液中的氢离子是水电离的为解答关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
3.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L的己烷所含的分子数为0.5 NA | |
| B. | 28 g乙烯所含共用电子对数目为4 NA | |
| C. | 0.1molCnH2n+2中含有的C-C键数为0.1n NA | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2 NA |
15.下列有关溶液的说法正确的是( )
| A. | 向10 mL pH=3的醋酸溶液中加入10 mL pH=11的NaOH溶液,混合液的pH=7 | |
| B. | 实验测定,NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>H2CO3 | |
| C. | NH4Cl溶液加水稀释过程中c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | 向AgI沉淀中加入饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
 于吸热反应的反应速率
于吸热反应的反应速率
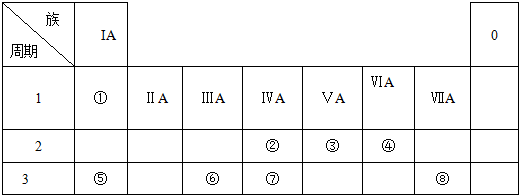
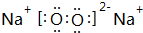 .
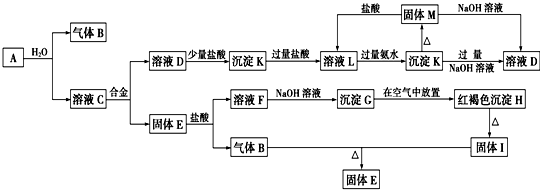
.
 .
.