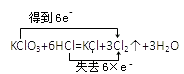
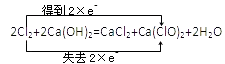题目内容
【题目】实验室制取乙炔的实验装置图(如图)中,
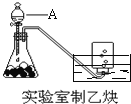
(1)A仪器的名称为_________________;所盛的试剂为_________________;发生反应的化学方程式为:__________________________________________________;
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是:_________________;将反应产生的乙炔通入溴的四氯化碳溶液中,反应的化学方程式为:__________________________________;(产物为1,2-二溴乙烯)
(3)生成的乙炔中可能含有的杂质气体是_________________,除去的方法是_________________。
【答案】 分液漏斗 饱和食盐水 CaC2+2H2O→Ca(OH)2+CH≡CH↑ 酸性高锰酸钾溶液紫色褪去 ![]() 硫化氢、磷化氢(H2S、PH3) 将混合气体通过CuSO4溶液洗气
硫化氢、磷化氢(H2S、PH3) 将混合气体通过CuSO4溶液洗气
【解析】试题分析:实验室用电石和水反应制取乙炔,由于该反应十分剧烈,所以通常用饱和食盐水代替水并通过分液漏斗控制滴加的速度来减小反应速率。由于电石中常含有硫化钙和磷化钙等杂质,故所制备的乙炔中会混有硫化氢和磷化氢等杂质而有臭味。
(1)A仪器的名称为分液漏斗;所盛的试剂为饱和食盐水;发生反应的化学方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑ ;
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是酸性高锰酸钾溶液紫色褪去;将反应产生的乙炔通入溴的四氯化碳溶液中,生成1,2-二溴乙烯的化学方程式为![]() ;
;
(3)生成的乙炔中可能含有的杂质气体是硫化氢、磷化氢(H2S、PH3),除去的方法是将混合气体通过CuSO4溶液洗气。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目