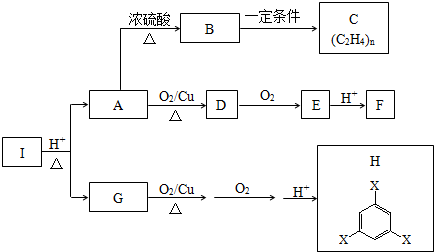
题目内容
13.下列化学反应的速率的说法中,正确的是( )| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 2mol/L 100ml的盐酸和锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢 | |
| D. | 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
分析 A.浓硫酸和铁发生钝化现象且不生成氢气,稀硫酸和铁反应生成氢气;
B.氢离子浓度越低反应速率越小;
C.无论放热反应还是吸热反应,升高温度都能增大反应速率;
D.对于气态参加的反应,减小压强,反应速率减小.
解答 解:A.铁在冷浓硫酸中发生钝化,加热时浓H2SO4与Fe反应不产生H2,故A错误;
B.加入适量的氯化钠溶液,体积增大,c(H+)减小,反应速率减小,故B错误;
C.升高温度,无论是放热反应,还是吸热反应,反应速率都增大,故C错误;
D.减小压强,对有气体参与的反应,反应速率减慢,故D正确.
故选D.
点评 本题考查化学反应速率影响因素,为高频考点,明确影响原理是解本题关键,易错选项是AC,注意浓硫酸、硝酸和铁反应都不生成氢气,注意升高温度能增大所有的化学反应速率,为易错点.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
3.在无色透明溶液,可大量共存的离子是( )
| A. | K+ Na+ OH- SO42- | B. | OHˉ SO42- Al3+ Cl- | ||
| C. | H+ Na+ CO32- Cl- | D. | K+ Na+ NO3- Cu2+ |
4.将碘水中的碘萃取出来的实验中,下列说法错误的是( )
| A. | 分液漏斗使用前要检查它是否漏水 | |
| B. | 萃取剂要求不溶于水,且比水更容易使碘溶解 | |
| C. | 分液时,下层液体应从下口流出,上层液体应从上口倒出 | |
| D. | 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后,不必静置,应立即分液 |
1.下列离子方程式书写正确的是( )
| A. | 铜跟硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 硫酸与氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 小苏打投入过量的澄清石灰水中 HCO3-+Ca2++OH-=CaCO3↓+H2O |
8.铀主要有两种同位素,关于${\;}_{92}^{235}U$的说法正确的是( )
| A. | 质子数为92 | B. | 中子数为235 | C. | 核外电子数为143 | D. | 质量数为92 |
18.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、Na+、SO42- | |
| B. | 水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
5.下列叙述中正确的是( )
| A. | 能导电的物质就是电解质 | |
| B. | 离子反应一定使溶液中所有离子的浓度都发生变化 | |
| C. | 复分解型离子反应必须具备有沉淀、气体、难电离的物质中之一的条件才能发生 | |
| D. | 酸碱中和反应都能用离子方程式:H++OH-=H2O表示 |
5.下列实验方案中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| B | 证明与苯环相连的甲基易被氧化 | 向2mL甲苯中加入3滴酸性KMnO4溶液,振荡;向2mL苯中加入3滴酸性KMnO4溶液,振荡,观察现象 |
| C | 比较HB和HA的酸性强弱 | 取等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体,观察收集到的气体哪个多 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
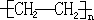 .反应类型是加聚反应.
.反应类型是加聚反应. _.
_.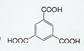 .
.