题目内容
【题目】纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油扭、涂料、密封胶与胶粘剂等行业.在浓CaCl2溶液中通人NH3和CO2 , 可以制得纳米级碳酸钙.某校学生实验小组设计下图所示装置制取该产品,D中装有稀硫酸的脱脂棉(图中夹持装置已略去).
I.可选用的药品有a.石灰石b.饱和氯化钙溶液c.6mol/L盐酸d.氯化铵固体e.氢氧化钙固体.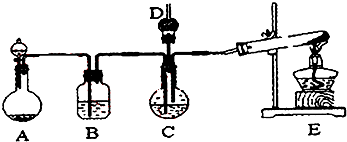
(1)A中制备气体时,所需药品是(选填字母序号);
(2)B中盛有溶液,其作用是;
(3)写出制取氨气的化学方程式;
(4)在实验过程中,向C中通入气体是有先后顺序的,应先通入的气体是(写化学式)
(5)检验D出口处是否有氨气逸出的方法是;
(6)写出制取纳米级碳酸钙的化学方程式 .
【答案】
(1)ac
(2)饱和碳酸氢钠;除去CO2中的HCl
(3)2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
(4)NH3
(5)将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出
(6)CaCl2+CO2+H2O+2NH3=2NH4Cl+CaCO3↓
【解析】解:(1.)装置A为制备二氧化碳装置,根据二氧化碳的实验室制法,可知装置中盛放的是碳酸钙和稀盐酸,即选择a、c,所以答案是:ac;
(2.)二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳,B中盛有饱和碳酸氢钠溶液,起到除去二氧化碳中的氯化氢的作用;所以答案是:饱和碳酸氢钠;除去CO2中的HCl;
(3.)氯化铵与氢氧化钙反应生成氯化钙、氨气和水,化学方程式为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑;所以答案是:2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑;所以答案是:2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
(4.)氨气极易溶于水,易于二氧化碳的吸收,所以应先通入氨气,所以答案是:NH3;
(5.)氨气能使湿润的红色石蕊试纸变蓝,所以检验氨气的方法:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;所以答案是:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;
(6.)氨气极易溶于水,二氧化碳不易溶于水,所以应先通入氨气;氨气溶于水生成氨水,溶液呈碱性,二氧化碳是酸性气体,能和碱反应生成碳酸铵,碳酸铵和氯化钙发生复分解反应生成碳酸钙和氯化铵CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl.所以答案是CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl.
【考点精析】掌握氨的实验室制法是解答本题的根本,需要知道安验室制法:用铵盐与碱共热,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O.