题目内容
常温下,有甲、乙两份体积均为1 L、浓度均为0.1 mol/L的氨水,其pH为11。①甲用蒸馏水稀释100倍后,溶液的pH变为a;②乙与等体积、浓度为0.2 mol/L的盐酸混合,在混合溶液中:n(NH4+ )+n(H+)-n(OH-) =" b" mol。则a、b正确的答案组合是
| A.9~11之间;0.1 | B.9~11之间;0.2 |
| C.12~13之间;0.2 | D.13;0.1 |
B
溶液稀释后,pH向7的方向过渡,若是强碱,稀释100倍后pH会从11→9,现是弱碱,所以pH为11~9之间,排除C、D二选项。在②中,〖思路一〗盐酸过量,n(OH-)很小,忽略不计,所以b = n(NH4+ )+n(H+) =" 0.1" mol+0.1 mol =" 0.2" mol,选B;〖思路二〗由电荷守恒n(NH4+ )+n(H+) = n(OH-)+n(Cl-),得:n(NH4+ )+n(H+)-n(OH-) = n(Cl-) =" b" =" 0.2" mol,选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
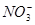 、Cl-
、Cl-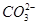 、OH-
、OH-