题目内容
工业生产硫酸过程中的一步反应是2SO2(g)+O2(g)?2SO3(g).如果该反应在密闭容器内进行,能说明该反应达到化学平衡状态的是( )
分析:可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析.注意选择的物理量随反应进行由变化到不变,说明到达平衡.
解答:解:A.可逆反应,反应物不能完全转化,故A错误;
B.消耗2mol SO2的同时生成2mol SO3,都表示正反应速率,反应始终按此比例进行,故B错误;
C.平衡时各物质的物质的量的多少取决于起始量与转化的程度,不能作为判断达到平衡的依据,故C错误;
D.平衡时各组分的浓度不再发生变化,SO2、O2与SO3 的浓度不再随时间变化,说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
B.消耗2mol SO2的同时生成2mol SO3,都表示正反应速率,反应始终按此比例进行,故B错误;
C.平衡时各物质的物质的量的多少取决于起始量与转化的程度,不能作为判断达到平衡的依据,故C错误;
D.平衡时各组分的浓度不再发生变化,SO2、O2与SO3 的浓度不再随时间变化,说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大,注意把握判断的角度以及平衡状态的特征,注意选择的物理量随反应进行由变化到不变,说明到达平衡.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
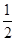 O2(g)?==?SO3(g) ΔH=+98.3 kJ·mol-1
O2(g)?==?SO3(g) ΔH=+98.3 kJ·mol-1