题目内容
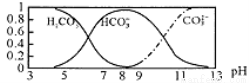
常温下,实验测得1.0mol/LNH4HCO3溶液pH=8.0。平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示。下列说法正确的是
A. 常温下Ka1(H2CO3)>Kb(NH3·H2O)>Ka2(H2CO3)
B. pH=13时,溶液中不存在HCO3-的水解平衡
C. pH由8~11时,c(CO32-)·c(H+)/c(HCO3-)不变
D. pH=3时,有c(NH4+)+c(NH3·H2O) =c(HCO3-)+c(CO32-)+c(H2CO3)
练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目


 [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
 z C(g)平衡时测得A的浓度为 0.5 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为 0.2mol·L-1,下列判断正确的是
z C(g)平衡时测得A的浓度为 0.5 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为 0.2mol·L-1,下列判断正确的是