题目内容
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O(相对分子质量为376)是一种氧气吸收剂,为红棕色晶体,潮湿时易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如下:

①待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
②将装置乙中混合物快速过滤、洗涤和干燥,称量得到 [Cr(CH3COO)2]2·2H2O。
③检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液。
④关闭K2,打开K1,旋开分液漏斗的旋塞并控制好滴速。
(1)正确的实验步骤为:______________________。
(2)步骤④的目的是_______________。
(3)三颈烧瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为________ 。
(4)实现步骤①中溶液自动转移至装置乙中的实验操作为__________________。
(5)洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是_______(填标号)
A.去氧冷的蒸馏水 B无水乙醇 C乙醚
(6)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51 g,实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.48 g,则该实验所得产品的产率为________(不考虑溶解的醋酸亚铬水合物)(用百分数表示,保留3位有效数字)。
【答案】③④①② 让锌粒与盐酸先反应产生H2,把装置2和3中的空气赶出,避免生成的亚铬离子被氧化 Zn + 2Cr3+ == Zn2+ +2 Cr2+ 关闭K1,打开K2 ABC 84.0%
【解析】
(1)第一步要检查装置气密性,第二步关闭K2,打开K1,第三步待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞,最后一步装置乙中混合物快速过滤、洗涤和干燥,称量得到 [Cr(CH3COO)2]2·2H2O。
(2)步骤④的目的是让锌粒与盐酸先反应产生H2,把装置2和3中的空气赶出,避免生成的亚铬离子被氧化。
(3)装置甲:分液漏斗盛装稀盐酸,在圆底烧瓶中和Zn反应Zn+2HCl=ZnCl2+H2↑,同时发生Zn + 2CrCl3 =2CrCl2+2ZnCl2。
(4)实验开始生成氢气后,为使生成的CrCl2溶液与醋酸钠溶液顺利混合,关闭K1,打开K2 ,把生成的CrCl2溶液压入装置乙中反应。
(5)醋酸亚铬水合物不溶于冷水和醚,微溶于醇,易溶于盐酸。
(6)CrCl3为9.51 g/158.5g/mol=0.06mol,得到CrCl2为0.06mol,根据原子守恒,则得到[Cr(CH3COO)2]2·2H2O为0.06mol。
(1)第一步要检查装置气密性,第二步关闭K2,打开K1,第三步待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞,最后一步装置乙中混合物快速过滤、洗涤和干燥,称量得到 [Cr(CH3COO)2]2·2H2O。故答案为:③④①② 。
(2)步骤④的目的是让锌粒与盐酸先反应产生H2,把装置2和3中的空气赶出,避免生成的亚铬离子被氧化,故答案为:让锌粒与盐酸先反应产生H2,把装置2和3中的空气赶出,避免生成的亚铬离子被氧化。
(3)装置甲:分液漏斗盛装稀盐酸,在圆底烧瓶中和Zn反应Zn+2HCl=ZnCl2+H2↑,同时发生Zn + 2CrCl3 =2CrCl2+2ZnCl2,该反应的离子方程式为:Zn + 2Cr3+ == Zn2+ +2 Cr2+,故答案为:Zn + 2Cr3+ == Zn2+ +2 Cr2+。
(4)实验开始生成氢气后,为使生成的CrCl2溶液与醋酸钠溶液顺利混合,关闭K1,打开K2 ,把生成的CrCl2溶液压入装置乙中反应,故答案为:关闭K1,打开K2 。
(5)醋酸亚铬水合物不溶于冷水和醚,微溶于醇,易溶于盐酸,所以可以选用冷水和乙醚
洗涤[Cr(CH3COO)2]2·2H2O产品,最后再用乙醚洗涤干燥,故答案为:ABC。
(6)CrCl3为9.51 g/158.5g/mol=0.06mol,得到CrCl2为0.06mol,根据原子守恒,则得到[Cr(CH3COO)2]2·2H2O为0.06mol,质量为0.06mol×1/2×376 g/mol=11.28g,所得产品产率为(9.48 g/11.28g)×100%≈84.0%,故答案为:84.0%。

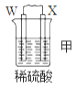
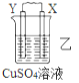
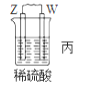
【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
装置 |
|
|
|
现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
A. 装置甲中W作原电池负极
B. 装置乙中Y电极上的反应式为Cu2++2e=Cu
C. 装置丙中溶液的pH减小
D. 四种金属的活动性强弱顺序为Z>W>X>Y