题目内容
【题目】高纯度镍是许多有机反应的催化剂。某化学课题组拟以电镀废液(含有NiS04、CuSO4和FeSO4)为原料,设计提取高纯镍的简单工艺如下(阴离子省略):

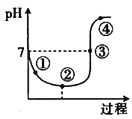
注:Ni(OH)2开始沉淀时的pH=7。
(1)加入新制氯水所发生反应的离子方程式为____
(2)加入NiCO3的目的是________。
(3)由氧化镍制备高纯度镍,有两种方案:
方案1:氧化镍溶于稀硫酸,加入足量锌粉,过滤、洗涤、干燥。
方案2:锌与稀硫酸反应产生氢气,氢气还原氧化镍。
制备等质量的镍粉,从消耗原料量、产品纯度、实验安全角度评价两种方案的优点。
方案1.____
方案2.____
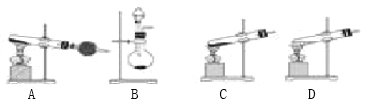
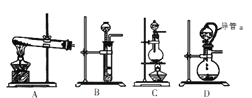
(4)方案2所用的氢气可以选用下列装置中的____来制取(填写字母,下同),收集氢气可选用装置________。
(5)若将D装置和E装置相连制取并收集干燥纯净的X气体,则X气体可以是下列气体中的____。装置D中导管a的作用是____。
a.CO2 b.Cl2 c.NO d.SO2

【答案】 Cl2+2Fe2+===2Fe3++2Cl- 调节溶液pH=3.7,使溶液中的Fe3+完全变成Fe(OH)3沉淀而除去 方案1:节省原料、实验安全 方案2:产品纯度较高 BD FH a d 平衡分液漏斗和烧瓶中的气压,便于分液漏斗中液体顺利流下
【解析】(1)分析题给流程知电镀废液加入新制氯水Fe2+被氧化为Fe3+,发生反应的离子方程式为Cl2+2Fe2+===2Fe3++2Cl-;(2)结合题给工艺流程和信息知加入NiCO3的目的是调节溶液pH=3.7,使溶液中的 Fe3+完全变成Fe(OH)3沉淀而除去;(3)方案1:操作简便、节省原料、实验安全。方案2:产品纯度较高;(4)锌与稀硫酸反应制备氢气为固体和液体不加热制备气体,可选用装置中的BD来制取;氢气难溶于水,可用排水法收集,氢气密度比空气小且与空气中的成分不反应,可用向下排空气法收集,故收集氢气可选用FH装置;(5)根据装置D装置和E装置的特点及气体的性质分析,该装置反应装置适用于制备固体与液体不加热反应制气体,可制取并收集干燥纯净的二氧化碳和二氧化硫,答案选ad;装置D中导管a的作用是平衡分液漏斗和烧瓶中的气压,便于分液漏斗中液体顺利流下。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。
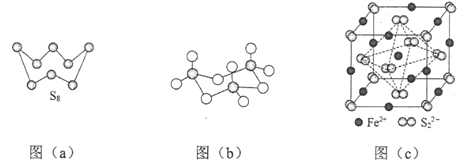
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。