题目内容
13. 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)═N2O4(g) (无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)═N2O4(g) (无色),如图所示.(1)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18mol/(L•min),乙中v(N2O4)=0.2mol/(L•s),则乙中反应更快.
(2)在0到1min中内用X表示该反应的速率是0.1mol•(L•min)-1,该反应达限度时,Y的转化率60%,反应开始时与反应达平衡状态时的压强之比为14:11.
分析 (1)根据反应速率之比等于化学计量数之比比较;
(2)根据v=$\frac{△c}{△t}$计算反应速率,结合图象计算相关物理量.
解答 解:(1)甲中v(NO2)=18mol/(L•min),乙中v (N2O4)=0.2mol•L-1•min-1,v(NO2)=2v(N2O4)=0.4mol•L-1•s-1=24mol/(L•min),则乙反应较快,
故答案为:乙;
(2)v(X)=$\frac{\frac{0.7mol-0.4mol}{2L}}{1min}$=0.15mol•(L•min)-1,
该反应达最大限度时,Y的转化率为:$\frac{1mol-0.4mol}{1mol}$=60%,
开始时:n(X)+n(Y)=0.4mol+1mol=1.4mol,
平衡时:n(X)+n(Y)=0.7mol+0.4mol=1.1mol,
在相同条件下,气体的压强之比等于物质的量之比,
则反应开始时与反应达平衡状态时的压强之比为1.4mol:1.1mol=14:11,
故答案为:0.1mol•(L•min)-1;60%;14:11.
点评 本题考查较为综合,题目难度中等,注意把握化学反应速率以及化学平衡的基本知识即可解答该题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.对于化学反应的限度的叙述,错误的是( )
| A. | 任何可逆反应都有一定的限度 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 相同条件下,不同的可逆反应,其反应的限度不同 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
4.金属的下列性质中,与金属的晶体结构无关的是( )
| A. | 易导电 | B. | 易导热 | C. | 有延展性 | D. | 易锈蚀 |
1.既可以用来鉴别乙烯和甲烷,又可以用来除去甲烷中混有的乙烯,得到纯净的甲烷的方法是( )
| A. | 通入酸性KMnO4溶液 | B. | 通入澄清石灰水 | ||
| C. | 通入足量的溴水 | D. | 通入浓硫酸 |
18.碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O═Zn(OH)2+Mn2O3,下列说法错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 电池工作时,电解质溶液中OH?的物质的量近似不变 |
5. 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积为
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
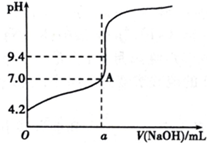
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(标准溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
2.下列关于常见有机化合物说法正确的是( )
| A. | 甲烷、乙烯和苯都可以从化石燃料中提取,都能使溴水因发生化学反应而褪色 | |
| B. | 乙烯和苯分子中因都存在C═C,因为都能发生加成反应和氧化反应 | |
| C. | 酸性KMnO4溶液既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 | |
| D. | 只用一种试剂就可以鉴别乙醇、乙酸、四氯化碳、苯四种液体 |
17.下列说法正确的是( )
| A. | 化学反应都是吸热反应 | |
| B. | 化学反应都是放热反应 | |
| C. | 物质发生化学反应都伴随着能量变化 | |
| D. | 有能量变化的物质变化都是化学变化 |
 和
和 ⑤H2O和H2O2
⑤H2O和H2O2 .
.