题目内容
【题目】【化学―选修5:有机化学基础】
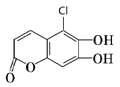
有机化合物G常用作香料。合成G的一种路线如下:
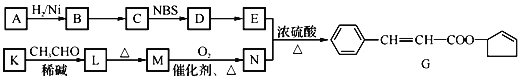
已知以下信息:
① A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢
② CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
③ CH3CHO+CH3CHO![]()
![]() 、
、![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
回答下列问题:
(1)A的结构简式为____________,D中官能团的名称为___________________。
(2)B→C的反应类型为_______________。
(3)D→E反应的化学方程式为__________________________________________。
(4)检验M是否已完全转化为N的实验操作是___________________________。
(5)满足下列条件的L的两种同分异构体有 ________种(不考虑立体异构)。① 能发生银镜反应 ② 能发生水解反应。其中核磁共振氢谱中有5组峰,且峰面积之比为1:2:2:2:3的结构简式为_________________。
(6)参照上述合成路线,设计一条以1-丁醇和NBS为原料制备顺丁橡胶(![]() )的合成路线:_________________________________。
)的合成路线:_________________________________。
【答案】 ![]() 碳碳双键、溴原子 消去反应
碳碳双键、溴原子 消去反应 ![]() +NaOH
+NaOH![]()
![]() +NaBr(或
+NaBr(或![]() +H2O
+H2O![]()
![]() +HBr) 取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N(或其他合理答案) 14
+HBr) 取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N(或其他合理答案) 14 ![]() 、
、![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2 ![]()
![]() (或其他合理答案)
(或其他合理答案)
【解析】由G的结构简式可知E、N分别为![]() 、
、![]() 中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为
中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为![]() ,E为
,E为![]() ,逆推可知M为
,逆推可知M为![]() ,L为
,L为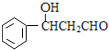 ,K为
,K为![]() .A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为
.A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为![]() ,则B为
,则B为![]() ,结合信息②可知,B发生消去反应生成C为
,结合信息②可知,B发生消去反应生成C为![]() ,C与NBS发生取代反应生成D为
,C与NBS发生取代反应生成D为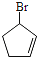 ,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
(1)由上述分析可知,A的结构简式为![]() ,D为
,D为![]() ,D中官能团的名称为:碳碳双键、溴原子;
,D中官能团的名称为:碳碳双键、溴原子;
(2)由上述分析可知,B→C的反应类型为消去反应;
(3)D→E反应的化学方程式为: ;
;
(4)M转化为N是醛基转化为羧基,可以检验反应后物质是否含有醛基判断M是否已完全转化为N,实验操作是:取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N;
(5)满足下列条件的L(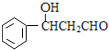 )的同分异构体:①能发生银镜反应,说明含有醛基,②能发生水解反应,含有甲酸形成的酯基,③属于芳香族化合物,含有苯环,含有一个取代基为-CH2CH2OOCH,或者为-CH(CH3)OOCH,含有2个取代基为-CH3、-CH2OOCH,或者为-CH2CH3、-OOCH,各有邻、间、对3种,可以含有3个取代基为2个-CH3、1个-OOCH,2个-CH3有邻、间、对3种,对应的-OOCH分别有2种、3种、1种位置,故符合条件的同分异构体共有14种,其中核磁共振氢谱中有5组峰,且峰面积之比为1:2:2:2:3的结构简式为
)的同分异构体:①能发生银镜反应,说明含有醛基,②能发生水解反应,含有甲酸形成的酯基,③属于芳香族化合物,含有苯环,含有一个取代基为-CH2CH2OOCH,或者为-CH(CH3)OOCH,含有2个取代基为-CH3、-CH2OOCH,或者为-CH2CH3、-OOCH,各有邻、间、对3种,可以含有3个取代基为2个-CH3、1个-OOCH,2个-CH3有邻、间、对3种,对应的-OOCH分别有2种、3种、1种位置,故符合条件的同分异构体共有14种,其中核磁共振氢谱中有5组峰,且峰面积之比为1:2:2:2:3的结构简式为![]() ;
;
(6)参照上述合成路线,设计一条以1-丁醇和NBS为原料制备顺丁橡胶(![]() )的合成路线:CH3CH2CH2CH2OH
)的合成路线:CH3CH2CH2CH2OH![]() CH3CH2CH=CH2
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2![]() CH2=CHCH=CH2
CH2=CHCH=CH2 ![]()
![]() 。
。

【题目】H2S 在金属离子的鉴定分析、煤化工等领域都有重要应用。请回答:
(一)H2S 是煤化工原料气脱硫过程的重要中间体。反应原理为
①COS(g)+H2(g)![]() H2S(g)+CO(g) △H=+7kJ/mol
H2S(g)+CO(g) △H=+7kJ/mol
②CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-42kJ/mol
CO2(g)+H2(g) △H=-42kJ/mol
已知断裂 1mol 气态分子中的化学键所需能量如下表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/kJ/mol | 1310 | 442 | x | 678 | 930 | 1606 |
(1)计算表中 x=____________。
(2)向VL容积不变的密闭容器中充入1molCOS(g)、amolH2(g)和1molH2O(g),发生上述两个反应,其他条件不变时,容器内CO的平衡体积分数与温度(T)的关系如下图所示。

已知:TIK时测得平衡体系中COS为0.80mol,H2为0.85mol。
① 随着温度的升高,CO的平衡体积分数增大,理由是____________。
② a=______。T1K时CO的平衡转化率为_______
③ T1K 时容器内总压强为pMPa,用气体分压代替气体浓度计算反应l 压强平衡常数Kp=____气体组分的分压=总压强×(气体组分的物质的量/气体总物质的量)(结果保留2位小数)。
(3)少量的羰基硫(COS)用氢氧化钠溶液处理的过程如下(部分产物已略去):
![]()
下图是反应Ⅱ中,在不同温度下,反应时间与H2产量的关系图(Na2S的初始含量为3mol),
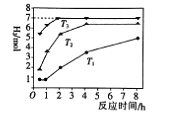
① Na2S溶液显_______(“酸性”或“碱性”)。
② 判断Tl、T2、T3的大小:_______。
(二)H2S 用于金属离子的鉴定。
(4)已知:25℃时,K(sp)(SnS)= 1.0×10-25, K(sp)(CdS)= 8.0×10-27。该温度下,向浓度均为0.1mol/L的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=______(溶液体积变化忽略不计)。
【题目】乙酸丁酯是重要的化工原料,具有水果香味。实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
物质 | 乙酸 | 正丁醇 | 乙酸丁酯 |
熔点/ ℃ | 16.6 | -89.5 | -73.5 |
沸点/ ℃ | 117.9 | 117 | 126.0 |
密度/g·cm-3 | 1.1 | 0.80 | 0.88 |
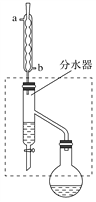
(1)乙酸丁酯粗产品的制备
在干燥的50 mL圆底烧瓶中,装入沸石,加入12.0 mL正丁醇和16.0 mL冰醋酸(过量),再加3~4滴浓硫酸。然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热。将烧瓶中反应后的混合物冷却与分水器的酯层合并。装置中冷水应从________(填“a”或“b”)管口通入;通过分水器下端旋塞分出的生成物是________,其目的是_____________________________。
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤。
①正确的操作步骤是________(填标号)。
A.①②③④ B.③①④②
C.①④①③② D.④①③②③
②分液漏斗有两种,如下图。分液时应选择下图中________形分液漏斗,其原因是_____________________________________________。

③蒸馏操作时,需收集________ ℃的馏分,沸点大于140 ℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是__________。