题目内容
【题目】〔化学——选修4:物质结构与性质〕
Ⅰ.铬位于第四周期ⅥB族,主要化合价+2,+3 ,+6,单质硬度大,耐腐蚀,是重要的合金材料。
(1)基态铬原子的价电子排布图_ ,CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子。
(2)CrCl3·6H2O实际上是配合物,配位数为6,其固体有三种颜色,其中一种浅绿色固体与足量硝酸银反应时,1mol固体可生成2mol氯化银沉淀,则这种浅绿色固体中阳离子的化学式 。
Ⅱ.砷化镓为第三代半导体材料,晶胞结构如图所示

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为 。
(4)AsH3空间构型为 。已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式是______________________。
(5)砷化镓晶体中最近的砷和镓原子核间距为a cm,砷化镓的摩尔质量为b g·mol-1,阿伏伽德罗常数值为NA,则砷化镓晶体密度表达式是 g·cm-3。
【答案】Ⅰ.(1)![]() 非极性
非极性
(2)[ Cr(H2O)5 Cl ]2+
Ⅱ.(3)(CH3)3Ga+AsH3![]() 3CH4+GaAs
3CH4+GaAs
(4)三角锥形 sp2 (5) 3![]() ·b/16a3NA
·b/16a3NA
【解析】
试题分析:(1)铬是24号元素,其原子核外有24个电子,3d能级上有4个电子、4s能级上有2个电子,3d、4s电子为其价电子,所以其价电子排布图为![]() ,CCl4、CS2都是非极性分子,非极性分子的溶质极易溶于非极性分子形成的溶剂,根据相似相溶原理知,CrO2Cl2是非极性分子。
,CCl4、CS2都是非极性分子,非极性分子的溶质极易溶于非极性分子形成的溶剂,根据相似相溶原理知,CrO2Cl2是非极性分子。
(2)1mol固体可生成2mol氯化银沉淀,说明该配合物的分子的外界有2个氯离子,则该配合物阳离子带两个单位的正电荷,其配位数是6,根据氯原子守恒知,则该配合物內界中含有1个氯原子和5个水分子,所以其阳离子为[ Cr(H2O)5 Cl ]2+ 。
(3)该反应为(CH3)3Ga和AsH3反应生成为GaAs,根据质量守恒可知还有CH4生成,所以反应的化学方程式为:(CH3)3Ga+AsH3![]() 3CH4+GaAs;
3CH4+GaAs;
(4)AsH3中含有3个δ键和1个孤电子对,空间构型为三角锥形,(CH3)3Ga中Ga形成3个δ键,没有孤电子对,为sp2杂化。
(5)AB、AC、AD、BC、BD、CD的边长相等,AF、BF的长相等为a,F位于体心上,O位于正三角形BCD的重心上,在正三角形BCD中,BE为三角形BCD的高,则CE为BC的一半,如图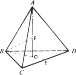 ,设正四面体的边长为x,CE的长为0.5x,BE=
,设正四面体的边长为x,CE的长为0.5x,BE=![]() ;BO与OE的长之比为2:1,则BO的长为
;BO与OE的长之比为2:1,则BO的长为![]() ,在三角形ABO中,AO的长为
,在三角形ABO中,AO的长为![]() ,在三角形BFO中,OF的长为
,在三角形BFO中,OF的长为![]() ,解得
,解得![]() ,正四面体的边长为x,对角线长2x,晶胞的棱长为
,正四面体的边长为x,对角线长2x,晶胞的棱长为![]() ,一个晶胞中含有4个砷化镓,所以密度表达式为
,一个晶胞中含有4个砷化镓,所以密度表达式为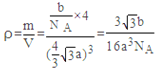 。
。

