题目内容
下列实验设计和结论正确的是( )
| A.向某溶液中加入盐酸后产生能使澄清石灰水变浑浊的无色无味气体,则该溶液一定含有CO32- |
| B.向饱和Na2CO3溶液中通入足量的CO2后溶液变浑浊,是因为析出了NaHCO3晶体 |
| C.向某溶液中加入适量新制氯水和几滴KSCN溶液后呈红色,则该溶液一定含有Fe2+ |
| D.向某溶液中滴加BaCl2溶液后产生不溶于稀硝酸的白色沉淀,则该溶液一定含有Ag+ |
B
试题分析:A、加入盐酸后产生能使澄清石灰水变浑浊的无色无味气体,溶液可能含有CO32?,也可能含有HCO3?,错误;B、NaHCO3的溶解度小于Na2CO3,正确;C、加入适量新制氯水和几滴KSCN溶液后呈红色,溶液可能含有Fe2+,也可能含有Fe3+,错误;D、滴加BaCl2溶液后产生不溶于稀硝酸的白色沉淀,则该溶液可能含有Ag+,也可能含有SO42?或SO32?,错误。

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目



 、
、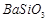 、
、 、
、 等]。某主要生产
等]。某主要生产 、
、 的化工厂利用钡泥制取
的化工厂利用钡泥制取 ,其部分工艺流程如下:
,其部分工艺流程如下:
 ,
, 的反应化学方程式为 。
的反应化学方程式为 。