题目内容
(6分)有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。
由上述现象推断:该混合物中一定含有 ;一定不含有 ;可能含有
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。
由上述现象推断:该混合物中一定含有 ;一定不含有 ;可能含有
(6分) Na2CO3 、Na2SO4、Ba(NO3)2 ; CuCl2、 K2CO3 ; NaCl
粉末溶于水得无色溶液和白色沉淀,说明一定没有CuCl2,一定含有Ba(NO3)2;在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明生成的白色沉淀是碳酸钡和硫酸钡;取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定没有K2CO3,所以一定含有Na2CO3 、Na2SO4,而氯化钠是不能确定的。

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO 、SO
、SO 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是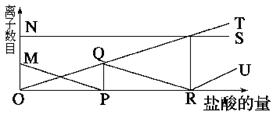
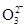 ; OT:HC
; OT:HC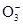 ; RU:Cl-
; RU:Cl-