题目内容
【题目】氰化钠(化学式NaCN,C元素+2价,N元素-3价)是白色结晶颗粒、易潮解、剧毒、易溶于水、水溶液呈碱性。氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
(1)氰化钠溶液呈碱性,其原因是 (用离子方程式解释)。
(2)用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式:________。
某化学兴趣小组在实验室制备硫代硫酸钠,并检测含氰化钠废水用硫代硫酸钠溶液处理后能否达标排放。
【实验一】实验室通过如下图所示装置制备Na2S2O3。

(3)装置a中盛装Na2 S03固体的仪器名称是 ,装置b的作用是________。
(4)装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有 (填化学式)。
(5)实验结束后,在e处最好连接盛____(填“NaOH溶液”“水”或“CCl4”)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg.L-l。
![]() ,AgI呈黄色,且CN-优先与Ag+反应,
,AgI呈黄色,且CN-优先与Ag+反应,
实验如下:取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000×1 0-4mol.L-l的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是________。
(7)处理后的废水中氰化钠的含量为 mg.L-l。
【答案】(1)CN-+H2O![]() HCN+OH-;(2)NaCN+H2O2+H2O=NH3↑+NaHCO3;(3)圆底烧瓶,安全瓶或防倒吸;(4)Na2SO4和Na2SO3;(5)NaOH溶液;(6)滴入最后一滴AgNO3溶液,出现黄色沉淀,且半分钟之内不消失;(7)0.98。
HCN+OH-;(2)NaCN+H2O2+H2O=NH3↑+NaHCO3;(3)圆底烧瓶,安全瓶或防倒吸;(4)Na2SO4和Na2SO3;(5)NaOH溶液;(6)滴入最后一滴AgNO3溶液,出现黄色沉淀,且半分钟之内不消失;(7)0.98。
【解析】
试题分析:(1)氰化钠溶液显碱性,说明氰化钠属于强碱弱酸盐,即CN-发生水解,CN-+H2O![]() HCN+OH-;(2)酸式盐只能是NaHCO3,气体能使湿润的红色石蕊试纸变蓝,说明此气体为NH3,因此反应方程式为H2O2+NaCN+H2O=NaHCO3+NH3↑;(3)盛放Na2SO3固体的仪器是圆底烧瓶,装置b的作用是安全瓶或防倒吸;(4)从装置c中,出来的气体中有SO2,被d吸收生成Na2SO3,Na2SO3容易被氧化成Na2SO4,因此可能有Na2SO3和Na2SO4;(5)根据信息,注射器是防止拆除装置时污染空气,即吸收SO2,SO2属于酸性气体,因此用NaOH吸收;(6)滴定到终点:滴入最后一滴AgNO3溶液,出现黄色沉淀,且半分钟之内不消失;(7)1L废水中含NaCN的质量是2.5×10-3×1×10-4×2×49×103/25×10-3g=0.98g,含量是0.98Mg·L-1。
HCN+OH-;(2)酸式盐只能是NaHCO3,气体能使湿润的红色石蕊试纸变蓝,说明此气体为NH3,因此反应方程式为H2O2+NaCN+H2O=NaHCO3+NH3↑;(3)盛放Na2SO3固体的仪器是圆底烧瓶,装置b的作用是安全瓶或防倒吸;(4)从装置c中,出来的气体中有SO2,被d吸收生成Na2SO3,Na2SO3容易被氧化成Na2SO4,因此可能有Na2SO3和Na2SO4;(5)根据信息,注射器是防止拆除装置时污染空气,即吸收SO2,SO2属于酸性气体,因此用NaOH吸收;(6)滴定到终点:滴入最后一滴AgNO3溶液,出现黄色沉淀,且半分钟之内不消失;(7)1L废水中含NaCN的质量是2.5×10-3×1×10-4×2×49×103/25×10-3g=0.98g,含量是0.98Mg·L-1。

【题目】某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
实验序号 | 锌的质量/g | 锌的状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 反应前溶液的温度/℃ | 其他试剂 |
1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
(1)在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过测定 进行判断,其速率最快的是 (填实验序号)。
(2)实验1和2表明 对反应速率有影响;实验1和3表明 对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。
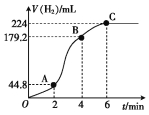
①在OA、AB、BC三段中反应速率最快的是 ,其原因是 。
②2~4 min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)v(H2SO4)= mol·L-1·min-1。
