题目内容
16.向纯水中加入少量的NaHSO4晶体,维持温度不变,则该溶液( )| A. | pH升高 | B. | pH降低 | ||
| C. | c(H+)、c(OH-)的乘积增大 | D. | pH维持不变 |
分析 硫酸氢钠是强电解质,在水溶液中完全电离,电离方程式为NaHSO4=Na++H++SO42-,相当于强酸溶液,温度不变,离子积常数不变,但溶液中氢离子浓度增大,据此分析解答.
解答 解:硫酸氢钠是强电解质,在水溶液中完全电离,电离方程式为NaHSO4=Na++H++SO42-,相当于强酸溶液,
A.溶液中氢离子浓度增大,则溶液的pH降低,故A错误;
B.根据A知,溶液的pH降低,故B正确;
C.温度不变,离子积常数不变,则该溶液中c(H+)、c(OH-)的乘积不变,硫酸氢钠抑制水电离,导致溶液中水电离出的c(H+)、c(OH-)的乘积减小,故C错误;
D.根据A知,溶液的pH降低,故D错误;
故选B.
点评 本题考查溶液pH计算,明确硫酸氢钠在水溶液中的电离特点是解本题关键,注意:离子积常数只与温度有关,与溶液酸碱性无关,易错选项是C.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
7.同分异构体现象在有机化学中是非常普遍的,下列互为同分异构体的是( )
①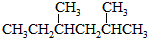 ②
②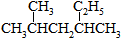 ③CH3CH2CH3
③CH3CH2CH3
④HC≡CCH3 ⑤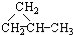 ⑥CH3CH=CHCH3.
⑥CH3CH=CHCH3.
①
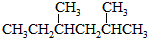 ②
②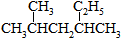 ③CH3CH2CH3
③CH3CH2CH3④HC≡CCH3 ⑤
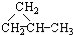 ⑥CH3CH=CHCH3.
⑥CH3CH=CHCH3.| A. | ①和② | B. | ①和③ | C. | ①和④ | D. | ⑤和⑥ |
4.25℃时,水的电离达到平衡,下列叙述正确的是( )
| A. | 向水中加人稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加人少量NH4Cl固体,c(OH-)增大 | |
| D. | 将水加热,Kw增大,pH不变 |
11.下列说法正确的是( )
| A. | 试管、烧杯、表面皿、蒸发皿、圆底烧瓶都能用酒精灯加热 | |
| B. | 用玻璃棒蘸取新制氯水,滴在pH试纸上,然后与比色卡对照,可测定新制氯水的pH值 | |
| C. | 向蛋白质溶液中加入硫酸铜溶液,可以使蛋白质变性 | |
| D. | 用标准NaOH溶液滴定盐酸,滴定管尖嘴部分在滴定前有气泡,滴定终点时无气泡,则测定结果将偏小 |
1.下列有关工业生产的叙述不正确的是( )
| A. | 用海水淡化后的浓缩海水作原料提取溴 | |
| B. | 在太阳能资源相对充足的沿海地区建造海水淡化厂 | |
| C. | 利用“海水→氯化钠→金属钠→氢氧化钠”的工艺流程生产烧碱 | |
| D. | 利用“海水→氢氧化镁→氯化镁→金属镁”的工艺流程生产金属镁 |
8.下列制取气体的方法可行的是( )
| A. | 制CO2:大理石+稀硫酸 | B. | 制SO2:Na2SO3(固)+浓硫酸 | ||
| C. | 制H2:Fe(固)+稀硝酸 | D. | 制Cl2:MnO2(固)+稀盐酸 |
5.环氧树脂具有极强的粘结性,俗称“万能胶”.双酚A是制备环氧树脂的重要原料,其结构为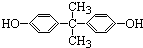 .下列有关双酚A的叙述不正确的是( )
.下列有关双酚A的叙述不正确的是( )
 .下列有关双酚A的叙述不正确的是( )
.下列有关双酚A的叙述不正确的是( )| A. | 不能和NaOH溶液反应 | B. | 能和FeCl3溶液反应显紫色 | ||
| C. | 能和浓溴水反应 | D. | 苯环上一溴代物有四种 |
6.下列叙述中不正确的是( )
| A. | 牛油、纤维素、蛋白质都是高分子化合物 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 棉花和人造丝的主要成分都是纤维素 | |
| D. | 浓硝酸和蛋白质发生反应可使皮肤呈黄色 |
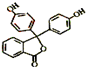 从其结构上看,酚酞属于酚或酯类衍生物,
从其结构上看,酚酞属于酚或酯类衍生物,