题目内容
2.最近报道在-100°C的低温下合成了化合物X,元素分析仪得出其分子式为C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别(一氯代物只有一种),而碳的化学环境(位置)却有2种,而且,分子中既有C-C单键,又有C=C双键.温度升高将迅速分解.X的结构简式是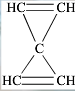 .
.
分析 根据“氢原子的化学环境没有区别”可知该有机物中所有氢原子都等效,再结合碳原子种类有2种,存在碳碳单键和碳碳双键判断有机物的结构式.
解答 解:有机物的分子式为:C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,则说明该分子中所有的H原子都是等效的;而碳的化学环境却有2种,即分子中含有2种位置不同的C,再结合分子中既有C-C单键,又有C=C双键可知,该有机物的结构简式为: ,故答案为:
,故答案为: .
.
点评 本题主要考查的是有机物的结构简式的确定,抓住“有1种化学环境的H,以及2种C”是解决本题的关键,有一定难度.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
12.下列实验操作中,正确的是( )
| A. | 用托盘天平称量药品时,左盘放药品,右盘放砝码 | |
| B. | 向试管中滴加试剂时,将滴管下端紧靠试管内壁 | |
| C. | 用燃着的酒精灯去点燃另一酒精灯 | |
| D. | 使用试纸检验溶液的性质时,将试纸浸入溶液中 |
13.下列说法错误的是( )
| A. | 主族元素的最外层电子数都等于它的最高正化合价 | |
| B. | 同一主族的元素的原子最外层电子数相等 | |
| C. | 同周期的主族元素随核电荷数的递增原子半径逐渐减小 | |
| D. | 第N周期有N种主族元素是金属元素(N>1) |
10.下列有关胶体的说法中,不正确的是( )
| A. | 胶体、溶液、浊液的分类依据是分散质微粒直径大小 | |
| B. | “卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关 | |
| C. | 向1 mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 | |
| D. | 可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体 |
17.已知可逆反应2SO2+O2 $?_{△}^{催化剂}$2SO3,当生成2mol SO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3放出的热量为Q1,则( )
| A. | Q1=Q | B. | Q1<Q | C. | 2Q1<Q | D. | 无法判断 |
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 某无色溶液中:Al3+、Cu2+、SO42-、Cl- | |
| B. | 由水电离的c(H+)=1×10-12 mol•L-1的溶液中:Fe2+、K+、Cl-、NO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Na+、Mg2+、NO3-、Cl- | |
| D. | 含有大量HCO3-的溶液中:NH4+、Al3+、Ca2+、Cl- |
14.下列说法中正确的是( )
| A. | 纯净物中一定存在化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中可能含共价键,共价化合物中不含离子键 |
11.下列各组元素的性质递变情况错误的是( )
| A. | Li、C、O原子最外层电子数依次增加 | B. | P、S、Cl元素最高正化合价依次升高 | ||
| C. | N、O、F原子半径依次增大 | D. | Li、Na、K的金属性依次增强 |