题目内容
16.为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于足量的稀盐酸,充分反应后,再进行下列实验,其结论正确的是( )| A. | 若再滴加KSCN溶液,溶液未变红,说明铁粉未变质 | |
| B. | 若再依次滴加氯水、KSCN溶液,溶液变红,说明铁粉部分变质 | |
| C. | 若再滴加KSCN溶液,溶液变红,说明铁粉部分变质或全部变质 | |
| D. | 若再滴加KSCN溶液,溶液未变红,再滴加氯水,溶液变红,说明铁粉全部变质 |
分析 Fe粉变质生成Fe2+或Fe3+,还原铁粉溶于稀盐酸时,溶液中含有Fe2+或Fe3+或二者都有,实验室采用酸性高锰酸钾溶液检验Fe2+,用KSCN溶液检验Fe3+,Fe2+具有还原性,能被强氧化剂氧化,据此分析解答.
解答 解:A.若再滴加KSCN溶液,溶液未变红,说明溶液中无Fe3+,但还原铁粉有可能被氧化为Fe2+,故A错误;
B.氯水具有强氧化性,可以把Fe2+氧化为Fe3+,Fe2+来源可能是铁与盐酸反应,故不能确定是部分氧化还是全部氧化还是没有被氧化,故B错误;
C.若再滴加KSCN溶液,溶液变红,证明含有Fe3+,则说明铁粉部分变质或全部变质,故C正确;
D.若再滴加KSCN溶液,溶液未变红,说明不含Fe3+,再滴加氯水,溶液变红,说明含有Fe2+,此现象说明铁粉部分变质或未变质,故D错误;
故选C.
点评 本题以铁离子、亚铁离子检验为载体考查物质检验和鉴别方法,为高频考点,明确物质性质是解本题关键,知道常见离子检验方法、操作步骤及现象,要排除其它离子干扰,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
16.下列四幅图中,与胶体性质有关的是( )


| A. | ①④ | B. | ②③ | C. | ①②③ | D. | 全部 |
7.从绿色化学和经济效益角度考虑,制取Cu(NO3)2最适宜采用的方法是( )
| A. | Cu+HNO3(浓)→Cu(NO3)2 | B. | Cu+HNO3(稀)→Cu(NO3)2 | ||
| C. | Cu$\stackrel{空气}{→}$CuO$\stackrel{稀硝酸}{→}$Cu(NO3)2 | D. | Cu+AgNO3→Cu(NO3)2 |
4.下列说法正确的是( )
| A. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性均依次减弱 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | NH5中的所有原子的最外层都符合相应稀有气体原子电子层结构,1molNH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值) |
11.下列化学用语正确的是( )
| A. | F-的结构示意图: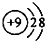 | B. | 乙烯分子比例模型: | ||
| C. | 乙酸的结构式:C2H4O2 | D. | Na2O的电子式: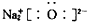 |
1.在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为产物,即原子利用率为100%.下列反应类型能体现原子利用率为100%的是( )
①取代反应②消去反应③加成反应④酯化反应⑤缩聚反应⑥加聚反应.
①取代反应②消去反应③加成反应④酯化反应⑤缩聚反应⑥加聚反应.
| A. | ②⑤ | B. | ①④ | C. | ③⑥ | D. | ⑤⑥ |
8.下列涉及有机物的说法正确的是( )
| A. | 冰醋酸与食用醋有相同的气味 | |
| B. | 乙烯、氯乙烯、苯乙烯都可用于合成有机高分子材料 | |
| C. | 苯能与溴发生反应,因此不能用苯萃取溴水中的溴 | |
| D. | 淀粉和纤维素水解的最终产物都是葡萄糖,因此二者互为同分异构体 |
6.氯气是一种重要的工业原料.工业上利用反应:3Cl2+2NH3→N2+6HCl 检查氯气管道是否漏气,有关说法中错误的是( )
| A. | 该反应利用了Cl2的强氧化性 | B. | 若管道漏气遇氨就会产生白烟 | ||
| C. | 该反应属于复分解反应 | D. | 生成1molN2有6mol电子转移 |
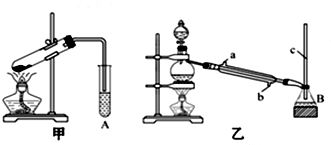
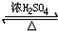 HCO18OCH3+H2O.
HCO18OCH3+H2O.