题目内容
下列一句话中叙述了两个值,前者记为M,后者记为N,M和N的关系从A、B、C、D 中选择:
A.M>N B.M<N C. M="N" D. 无法比较
(1)相同温度下,1L 1mol/L 的NH4Cl溶液和2 L 0.5mol·L-1NH4Cl溶液,两溶液中NH4+的个数: ;
(2)相同温度下,pH值为12的烧碱溶液和CH3COONa溶液,两溶液中水的电离程度: ;
(3)常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-): ;
(4)将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值: ;
(1)A (2)B (3)B (4)B
解析试题分析:(1)氯化铵中,铵根离子水解,铵根离子浓度越大水解程度越小,即相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数大于2L 0.5mol?L-1NH4Cl溶液中NH4+的个数,故答案为:A;(2)pH值为12的烧碱溶液中水电离出的氢离子浓度为10-12mol/L,pH值为12的CH3COONa溶液中水电离出的氢离子浓度为10-2mool/L,所以相同温度下,pH值为12的烧碱溶液中水的电离度小于pH值为12的CH3COONa溶液中水的电离度,故答案为:B;(3)碳酸钠溶液中,碳酸根的水解程度随着温度的升高而增大,及升高温度以黄埔,碳酸氢根的浓度增大,故答案为:B;(4)醋酸是弱酸,稀释促进电离,盐酸是强酸,稀释过程浓度减小,所以将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值是醋酸的小于盐酸的,故答案为:B;
考点:影响盐类水解程度的主要因素;有关ph的计算

练习册系列答案
相关题目
结合下表回答下列问题(均为常温下的数据):
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| HClO | 3×10-8 |
(1)上述三种酸中,酸性最强的是 。
(2)在常温下,相同物质的量浓度的①CH3COONa、 ②Na2CO3、③NaClO三种溶液的pH由小到大的顺序为 。(用序号回答)
(3)设计一个现象明显、操作简便的实验方案证明CH3COOH酸性强于碳酸(不用叙述仪器和具体操作) 。
(4)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的钠盐,同时还有另两种钠盐生成,该反应的化学方程式为 。
(5)实验证明:向0.01 mol/L NaAlO2溶液中加入等体积0.01 mol/L NaHCO3溶液,会产生白色胶状沉淀。据此推断CO32-和AlO2-两种离子中,结合质子(H+)能力较强的是 。
 Fe(OH)3+3HC1;△H>0。回答下列问题:
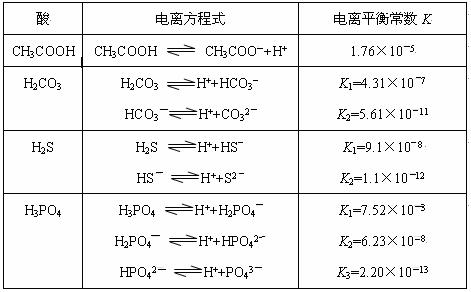
Fe(OH)3+3HC1;△H>0。回答下列问题: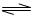 H++A―,则该弱酸的电离平衡常数的表达式为K=__________。下表是几种常见弱酸的电离平衡常数(25℃)。
H++A―,则该弱酸的电离平衡常数的表达式为K=__________。下表是几种常见弱酸的电离平衡常数(25℃)。