��Ŀ����
��11�֣� ��100mLij���۽���M���������������Һ�м��������NaHCO3��Һ��������MCO3���������ˣ����������������������У��ռ�����״����4.48L�����壻����Һ��ˮϡ�͵�250 mL��ȡ��25 mLǡ����20 mL������ȫ��Ӧ���ռ�����״����1.12 L�����塣��ش�
(1)M��OH��2�����NaHCO3��Һ��Ӧ�Ļ�ѧ����ʽΪ��
(2)Ҫ����M�����ԭ������������Ϊ�������ṩ������������ (ѡ����ĸ���)��
A.M������������Һ�����ʵ���Ũ��(��Ϊ2mol/L)
B.M��̼���ε�����(��Ϊ39.4 g)
C.��M��̼���η�Ӧ����������ʵ���Ũ��(��Ϊ0.1 mol/L)
D.�������ݳ��㣬����Ҫ�������ݡ�
�������ѡ�������M�����ԭ������Ϊ��
(3)������Һ��Ӧ����������ʵ���Ũ�ȡ�
(1)M(OH)2 +2NaHCO3=MCO3��+Na2CO3+2H2O ��2�֣�
(2��B��![]() 2�֣�
2�֣�
�⣺��Ϊ���������������CO2Ϊ4.48L(��״��)����������ʽ������
n(CO2)=n(MCO3)==0.2mol
M(MCO3)=[39.4g/0.2mol]=197g?mol��1
M�����ԭ������Ϊ��197-60=137��2�֣�
(3���⣺��Ϊ25mL��Һ�����ᷴӦ������CO2Ϊ1.12L(��״��)����������ʽ������
n(Na2CO3) +n(NaHCO3) =n(CO2)= 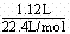 =0.05mol
=0.05mol
����25mL��Һ��n(Na2CO3)==0.02mol,����HCl 0.04mol
25mL��Һ��n(NaHCO3)=0.05mol-0.02mol=0.03mol������HCl 0.03mol
��c(HCl)==3.5mol?L-1
������Һ��Ӧ����������ʵ���Ũ��Ϊ3.5mol?L��1����5�֣�
