题目内容
向100mL某二价金属M的氢氧化物澄清溶液中加入过量的NaHCO3溶液,产生MCO3沉淀.过滤,将沉淀置于足量的盐酸溶液中,在标准状况下收集到4.48L气体.将滤液加水稀释至250mL,取出25mL,恰好与20mL盐酸反应,在标准状况下收集到1.12L气体.
(1)写出M的氢氧化物和碳酸氢钠反应的化学方程式________
(2)要计算出M的相对原子质量,你认为还必须提供下列哪些数据________(填写字母序号)
[ ]
A.M的氢氧化物溶液的物质的量浓度(设为2mol·L-1)
B.M的碳酸盐沉淀的质量(设为39.4g);
C.与M的碳酸盐反应的盐酸的物质的量浓度(设为0.1mol·L-1)
D.题设条件充足,不需要补充数据.
(3)根据你的选择,试计算金属M的相对原子质量和加入的NaHCO3溶液中溶质的质量.
答案:
解析:
解析:
|
(1)M(OH)2+2NaHCO3=MCO3↓+Na2CO3+2H2O (2)B (3)MCO3+2HCl=MCl2+CO2↑+H2O 1mol 22.4l x mol 4.48L x=0.2mol 因此碳酸盐摩尔质量为 因此M的相对原子质量为197-60=137 NaHCO3的物质的量为 其质量为84g·mol-1×0.7mol=58.8g |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 =197g·mol-1
=197g·mol-1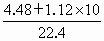 =0.7mol
=0.7mol