题目内容
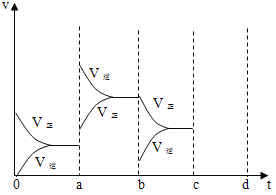
【题目】(1)下图表示在密闭容器中反应:2SO2+O2 ![]() 2SO3 △H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是_____;b→c 过程中改变的条件可能是_____; 若增大压强时,将反应速度变化情况画在 c~d 处____________。
2SO3 △H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是_____;b→c 过程中改变的条件可能是_____; 若增大压强时,将反应速度变化情况画在 c~d 处____________。
(2)可逆反应 mA(g)+nB(g)![]() pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
①用“>”、“=”或“<”填空:该反应的Δ H_____0,m+n_____p。
②用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入 B,则 A 的转化率_____;升高温度,则平衡时 B、C 的浓度之比 c(B)/c(C)将_____;加入催化剂,平衡时气体混合物的总物质的量_____。
③若 A、C 均为无色气体,B 为红色气体,用“变深”、“变浅”或“不变”填空:恒容下加入 C,平衡混合物的颜色_____;而恒压充入氖气,平衡混合物颜色_____。
【答案】升温减小 SO3 浓度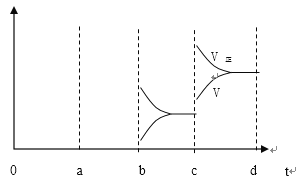 >>增大减小 不变变深变浅
>>增大减小 不变变深变浅
【解析】
(1)a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果;b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因;若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图像应为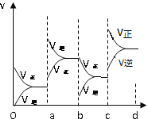 ;故答案为:升高温度;降低产物SO3浓度;
;故答案为:升高温度;降低产物SO3浓度;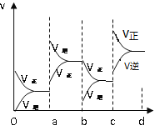 ;
;
(2)①当升高温度时,B的转化率变大,说明平衡向正反应移动,升高温度平衡向吸热反应移动,故正反应是吸热反应,减小压强时,混合体系中C的质量分数也减小,平衡向逆反应移动,减小压强平衡向气体体积增大的方向移动,即m+n>p,故答案为:>;>;
②加入B(体积不变),平衡向正反应移动,其它反应物的转化率增大,自身转化率降低,则A的转化率增大,升高温度平衡向正反应移动,平衡时B的浓度降低,C的浓度增大,所以则平衡时B、C的浓度之比![]() 将减小,催化剂不影响化学平衡状态,所以平衡时气体混合物的总物质的量不变,故答案为:增大;减小;不变;
将减小,催化剂不影响化学平衡状态,所以平衡时气体混合物的总物质的量不变,故答案为:增大;减小;不变;
③加入C(体积不变)时,平衡向逆反应方向进行,B的浓度增大,颜色变深;维持容器内压强不变,充入氖气,容器体积增大,B的浓度降低,颜色变浅,故答案为:变深;变浅。