题目内容
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一.其工艺流程如下: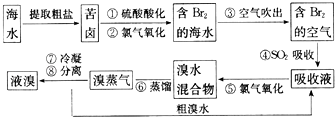
(1)溴在周期表中位于第周期,第族.
(2)步骤②中反应的离子方程式是 .
(3)步骤④利用了SO2的还原性,反应的离子方程式为 .
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离.分离仪器的名称是 .
【答案】
(1)4;VIIA
(2)2Br﹣+Cl2=Br2+2Cl﹣
(3)Br2+SO2+2H2O=4H++2Br﹣+SO42﹣
(4)分液漏斗
【解析】解:(1)因溴在氯的下一周期,与氯在同一主族,所以溴在周期表中位于第4周期VIIA族,所以答案是:4;VIIA;(2)步骤②为氯气与溴离子反应生成溴单质,反应的离子方程式为:2Br﹣+Cl2=Br2+2Cl﹣ , 所以答案是:2Br﹣+Cl2=Br2+2Cl﹣;(3)SO2和溴单质、水反应生成硫酸和氢溴酸,反应的离子方程式为:Br2+SO2+2H2O=4H++2Br﹣+SO42﹣ , 所以答案是:Br2+SO2+2H2O=4H++2Br﹣+SO42﹣;(4)因液溴与溴水不相溶,可用分液漏斗通过分液操作分离,所以答案是:分液漏斗.

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案【题目】实验室制备1,2﹣二溴乙烷的反应原理如下: CH3CH2OH ![]() CH2═CH2
CH2═CH2
CH2═CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母) a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 , 其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母) a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是;
(4)将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”);
(5)若产物中有少量未反应的Br2 , 最好用洗涤除去;(填正确选项前的字母) a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是