题目内容
下列各组物质中,Y是X物质中含有的少量杂质,Z是除杂试剂,其中所加试剂最合理的一组是( )
| X | Y | Z |
A | CO2 | SO2 | 饱和Na2CO3溶液 |
B | HCl | Cl2 | 饱和NaCl溶液 |
C | Fe2O3 | Al2O3 | NaOH溶液 |
D | Na2SO4溶液 | Na2CO3 | 盐酸 |
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
物质 组别 | 甲 | 乙 | 丙 |
A | Mg | FeSO4 | O2 |
B | Cl2 | H2O | NH3 |
C | Fe | H2O | FeCl3 |
D | NaHCO3 | Ca(OH)2 | Na2CO3 |



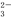 +I2=S4O
+I2=S4O +2I-)
+2I-)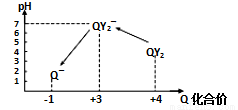





 石灰水、硅酸钠溶液,选择所给试剂,用如上图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
石灰水、硅酸钠溶液,选择所给试剂,用如上图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性) 通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2 (填序号)。
通入到饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2 (填序号)。