题目内容
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是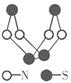
| A.该物质的分子式为SN | B.该物质的晶体中微粒间作用力有2种 |
| C.该物质具有很高的熔、沸点 | D.该物质与化合物S2N2互为同素异形体 |
B
解析

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
下列变化中,吸收的热量用于克服分子间作用力的是
| A.加热金属铝使之熔化 |
| B.加热金刚石使之熔化 |
| C.液溴受热变成溴蒸气 |
| D.加热碘化氢使之分解 |
下列物质中含有共价键的离子化合物是( )
| A.Ba(OH)2 | B.CaCl2 | C.H2O | D.H2 |
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H= - 602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
能用键能知识解释的是
| A.稀有气体的化学性质很不活泼 | B.HCl气体比HI气体稳定 |
| C.干冰易升华 | D.HF熔沸点高于HCl |
PH3是一种无色剧毒气体,其分子结构和NH3相似。下列判断错误的是( )
| A.PH3分子呈三角锥形 |
| B.PH3分子是极性分子 |
| C.PH3分子中所有原子最外层都满足8e—结构 |
| D.PH3分子稳定性低于NH3分子,因为N-H键键长更短、键能更高 |
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108.1°,下列有关N(NO2)3的说法正确的是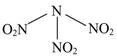
| A.分子中N、O间形成的共价键是非极性键 | B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 | D.15.2 g该物质含有6.02×1022个原子 |
下列关于化学键的叙述,正确的一项是( )
| A.离子化合物中一定含有离子键 |
| B.单质分子中均不存在化学键 |
| C.含有极性键的分子一定是极性分子 |
| D.含有共价键的化合物一定是共价化合 |
下列各物质中,化学键类型完全相同的是
| A.Na2O2和NaOH | B.CH3COONa和NaOH |
| C.CCl4和H2O | D.CO2和H2O2 |