题目内容
在无色透明的酸性溶液中,能大量共存的离子组是( )
| A.Na+、Ag+、S2-、SO42- | B.Mg2+、NH4+、NO3- 、Cl- |
| C.Na+、K + 、SO32-、CH3COO- | D.Cu2+、Na+、NO3-、SO42- |
B
解析试题分析:A Ag+、S2-、SO42-会反应生成AgS、Ag2SO4沉淀而不能共存。错误。B 不会发生任何反应,可共存,正确。C 在酸性条件下CH3COO- 不能存在。错误。D Cu2+有颜色,错误。
考点:离子反应、离子共存等知识。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
某强碱性溶液中,能大量共存的离子组是
| A.K+、Na+、AlO2-、SO42- | B.K+、Na+、ClO-、S2- |
| C.Na+、K+、SO42-、HCO3- | D.Ca2+、K+、NO3-、I- |
现有E、F、G、M、N五种可溶的强电解质,它们在水中电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
①E、F两溶液呈碱性;G、M、N 溶液呈酸性。
②向N溶液中逐滴滴加F溶液至过量,沉淀量先增加后减少但不消失。
③M溶液与另外四种溶液反应都能产生沉淀。
下列说法正确的是
A.N溶液与过量的F溶液反应的离子方程式: Ba2++SO42-=BaSO4↓
B.E溶液与N溶液混合发生反应:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
C.M溶液与F溶液混合产生的沉淀不能溶解于过量氨水中
D.将G溶液逐滴加入等体积、等物质的量的浓度的E溶液中,反应的离子方程式为
2H++CO32-=CO2↑+H2O
下列离子方程式表达正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HCO3-+H2O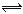 H3O++CO32- H3O++CO32- |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O |
下列物质中,属于电解质的是( )
| A.铜丝 | B.MgCl2 固体 | C.NaCl溶液 | D.酒精(C2H5OH) |
某无色溶液中含有K+,Cl-,OH-,SO32-,SO42-,为了检验除OH-外的其它所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象: 下列有关结论错误的是 ( )
下列有关结论错误的是 ( )
| A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl |
| B.现象3中白色沉淀是BaSO4 |
| C.试剂②是盐酸,试剂③是硝酸 |
| D.产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+SO42- |
下列可以大量共存且溶液是无色的离子组是( )
| A.H+、Na+、NO3-、Cu2+ | B.Ba2+、Mg2+、Cl-、SO42- |
| C.H+、K+、OH-、NO3- | D.NO3-、SO42-、K+、Mg2+ |
下列离子反应方程式正确的是
A.铜粉与98.3%的硫酸加热下反应:Cu + 4H+ + SO42― Cu2++ SO2↑+ 2H2O Cu2++ SO2↑+ 2H2O |
B.电解饱和食盐水:2Cl- +2H+ H2↑+C12↑ H2↑+C12↑ |
| C.向氯化铝溶液中加入过量氨水:Al3++ 4NH3·H2O=[Al(OH)4]-+ 4NH4+ |
| D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
在由水电离出的c(H+)=1×10-13 mol·L-1的溶液中一定大量共存的离子组是
| A.Fe2+、Na+、NO3-、Cl- | B.Ba2+、Na+、NO3-、Cl- |
| C.SO42-、SO32-、NH4+、Na+ | D.Mg2+、Na+、Br-、AlO2- |