题目内容
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是
A. Na+、Fe3+、NO3-、C12都可在该物质的溶液中大量共存
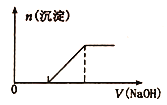
B. 向0. 1 mol/L该物质的溶液中逐滴滴加0. 1mol/L NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示
C. 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入儿滴KSCN溶液,观察溶液是否变红色
D. 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀的离子方程式为 Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓
【答案】C
【解析】试题分析:A.Fe2+ 有还原性,可被Cl2氧化为Fe3+而不能大量共存,错误;B.滴加NaOH溶液,首先是Fe2+ 先与OH反应生成白色沉淀,然后是发生反应:NH4++OH-=NH3H2O,图像与发生的反应事实不符合,错误;C.若Fe2+ 被氧化为变质为Fe3+,只需滴入几滴KSCN溶液,可观察到溶液变为红色,因此可鉴别,正确;D. 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42-完全沉淀的离子方程式为Fe2++ 2NH4++ 2SO42-+ 2Ba2++4OH-=2BaSO4↓+Fe(OH)2↓+2 NH3H2O,,漏掉NH4+与OH-的反应,故错误。

【题目】我国农业因酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定数据如下:
时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
根据上述材料回答下列问题:(已知Cl2+SO2+2H2O![]() H2SO4+2HCl)
H2SO4+2HCl)
①酸雨有很大的危害,严重威胁着生态环境。酸雨的PH____5.6(填< 或 >)。
②酸雨放置时,pH发生变化的主要原因是(用化学方程式表示)_____________________。
③如果将刚取样的上述雨水与少量新鲜自来水混合,pH将______(填“变大”、“变小”或“不变” )。
(2)你认为以下哪些做法是减少酸雨产生的途径_____________( 填序号)
①少用煤作燃料 ②把烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
(3)十二届全国人民代表大会政府工作报告中强调“加强雾霾治理,淘汰黄标车和老旧车”,下列物质不属于空气污染物的是 (______)
A. CO2 B. SO2 C. NO2 D. PM2.5
(4)改善大气质量、污水处理和实现垃圾的资源化等都要依靠化学等科学的发展。
固体煤气化得到CO和H2,在燃烧时可以大大减少________(填化学式,下同)和烟尘的排放。汽车尾气的主要污染是形成_______________,防止此种污染的措施是将汽车尾气中的CO、NO在催化剂的作用下反应生成无害的CO2和_____。