题目内容
硝酸是一种重要的工业原料,工业制硝酸的关键是氨的催化氧化,与硝酸工业相关的过程中产生的氮氧化物的处理与应用也是科学研究的热点。
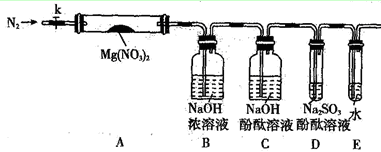
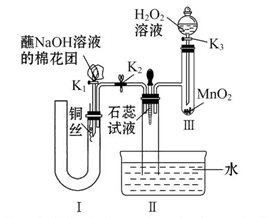
I.图10、图11分别是实验室模拟合成氨及氨催化氧化的装置
(1)氮气和氢气通过图10装置,该装置中浓硫酸的作用是控制气体流速和 。
(2)用图11装置吸收一段时间氨后,再通入空气,同时将已经加热的铂丝插入乙装置的锥形瓶内,铂丝保持红热的原因是 ,写出该装置中氨氧化的化学方程式 。反应结束后锥形瓶内的溶液中含有H+、OH-、 离子、 离子。
II.下列有关硝酸事实的解释合理的是
| A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定 |
| B.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化亚铁离子 |
| C.不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性 |
| D.不用锌与稀硝酸反应制取氢气,说明稀硝酸能将锌钝化 |
(1)工业上常用Na2CO3溶液吸收法处理NOx 。
已知:NO不能与Na2CO3溶液反应
NO + NO2 + Na2CO3 = 2NaNO2 + CO2 ①
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2 ②
用足量的Na2CO3溶液完全吸收NOx,每产生5.6L(标准状况)CO2(全部逸出)时,吸收液质量就增加10g,则NOx中的x值为 。
(2)尿素也可用于吸收处理NOx,其反应原理为:
NO+NO2+H2O=2HNO2
2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
当混合气体中NO、NO2按上述反应中系数比时吸收效果最佳。若混合气体中V(NO)∶V(NO2)=3∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)= (空气中氧气的体积含量约为20%)。
I.(1)干燥混合气体 (2分)
(2)氨的氧化反应是一个放热反应 (2分); 4NH3十5O2 4NO+6H2O。(2分)
4NO+6H2O。(2分)
NH4+ (1分), NO3- (1分)
II. A (2分)
(1) 1.75 (2分)
(2)5:6(2分)
解析试题分析;(1)浓硫酸具有干燥的作用所以(1)的答案为干燥混合气体(2)铂丝保持红热说明这个反应时放热反应,氨气溶于水形成氨水,故溶液中会存在铵根离子,一氧化氮会被氧气氧化生成二氧化氮,二氧化氮溶于水生产硝酸,故溶液中会存在硝酸根离子。II.硝酸不管是稀得还是浓的他都具有强的氧化性,故B选项是错误的。不用浓硝酸来制备硝酸铜主要是因为该反应会释放出污染大气的二氧化氮气体,与硝酸的挥发性无关,故C选项是错误的。而D选项主要是金属与硝酸反应不会生成氢气。所以答案选A(1)据题意可知2NOX—CO2,而逸出出来的二氧化碳为0.25摩尔即11克,故NOX为0.5摩尔,据题意可知NOX的质量为二氧化碳的质量加上碳酸钠溶液增加的质量即21克,再根据物质的量等于质量处于摩尔质量可求出X为1.75.(2)由题意可知一氧化氮与二氧化氮的比例关系为1;1时吸收效果最好由反应方程式2NO+O2=2NO2及题意,我们可以设一氧化氮转化成二氧化氮X摩尔,则3-X=1+X,推算得出X为1则。说明消耗氧气0.5摩尔即空气2.5摩尔。所以V(空气)∶V(NO)=5;6
考点:考查氮的氧化物的相关知识及计算

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
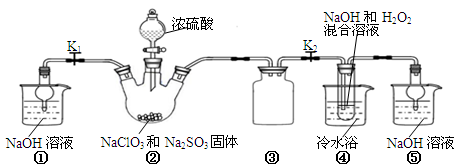
浙江新课程三维目标测评课时特训系列答案 (12分)某研究小组欲探究SO2的化学性质,设计了如下实验方案。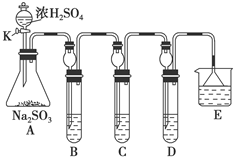
(1)在B中检验SO2的氧化性,则B中所盛试剂可为________。
(2)在C中装FeCl3溶液,检验SO2的还原性,则C中反应的离子方程式为__________________________。
(3)在D中装新制漂白粉浓溶液。通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分进行了探究。请回答下列问题:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1盐酸、0.5 mol·L-1H2SO4溶液、0.5 mol·L-1BaCl2溶液、品红溶液、新制澄清石灰水。
(ⅰ)假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为________;
假设三:该白色沉淀为上述两种物质的混合物。
(ⅱ)基于假设一,填写下表:
| 实验操作 | 预期现象和结论 |
| 将D中沉淀过滤,洗涤干净备用 | |
| 用另一干净试管取少量沉淀样品,加入 ______ | __________ |
__________________________________________________。
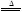 2KNO2+O2↑
2KNO2+O2↑ 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑ 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑