题目内容
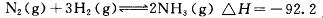 kJ
kJ 。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是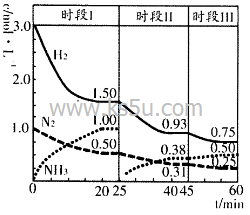
| A.前25min内反应放出的热量为46.lkJ |
| B.第25min改变的条件是将NH3从反应体系中分离出去 |
| C.若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.若时段I中投入物质的浓度为原来的2倍,则反应物的转化率增大,平衡常数不变 |
A
试题分析:A、前25min反应的N2为:0.50mol/L×2L=1mol,根据热化学方程式可知反应放出的热量为92.2kJ,错误;B、第25min NH3的浓度减小,而N2和H2的浓度随平衡的移动逐渐减小,所以改变的条件是将NH3从反应体系中分离出去,正确;C、平衡向正反应方向移动,而且N2、H2、NH3的浓度随着平衡的移动逐渐变化,所以时段Ⅲ改变的条件是降低温度,正确;D、若时段I中投入物质的浓度为原来的2 倍,容器内压强增大,平衡更有利于向正反应方向移动,反应物的转化率增大,但平衡常数不变,正确。

练习册系列答案
相关题目
 3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是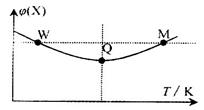
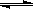 CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是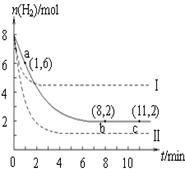
 N2(g)+CO2(g) △H="Q" kJ·mol-1在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H="Q" kJ·mol-1在T1℃时,反应进行到不同时间测得各物质的浓度如下:
 Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是 xC(g)+2D(g)。经5 min后达到平衡,平衡时测得D的浓度为0.5 mol·L-1,c(A):c(B) = 3:5,v(C) = 0.1 mol·L-1·min-1。
xC(g)+2D(g)。经5 min后达到平衡,平衡时测得D的浓度为0.5 mol·L-1,c(A):c(B) = 3:5,v(C) = 0.1 mol·L-1·min-1。