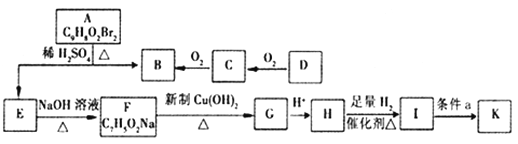
题目内容
【题目】氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常数Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定l0mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是

A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-,因此溶液呈碱性
B. C点所在溶液中 =2.5×10-5
=2.5×10-5
C. A、B、C、D四点溶液中,水电离出来的c(H+):C > D > B > A
D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-)
【答案】B
【解析】A. CH3NH2·H2O也是一元弱碱,甲胺在水中的电离不能完全进行,故A错误;B. C点硫酸与甲胺恰好完全反应,溶液中c(OH-)的负对数pOH=9,  =
=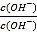 ×
×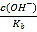 =
=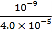 =
=![]() =2.5×10-5,故B正确;C. C点硫酸与甲胺恰好完全反应,生成的盐的浓度最大,对水的电离常见最大,D点硫酸电离的氢离子浓度大于A点甲胺电离的氢氧根离子浓度,对水的电离的抑制程度大,A、B、C、D四点溶液中,水电离出来的c(H+): C > B > A>D,故C错误;D. B点溶液中存在等物质的量浓度的盐和甲胺,溶液显碱性,以甲胺的电离为主,c(CH3NH3+)>c(CH3NH2·H2O)> c(H+)>c(OH-),故D错误;故选B。
=2.5×10-5,故B正确;C. C点硫酸与甲胺恰好完全反应,生成的盐的浓度最大,对水的电离常见最大,D点硫酸电离的氢离子浓度大于A点甲胺电离的氢氧根离子浓度,对水的电离的抑制程度大,A、B、C、D四点溶液中,水电离出来的c(H+): C > B > A>D,故C错误;D. B点溶液中存在等物质的量浓度的盐和甲胺,溶液显碱性,以甲胺的电离为主,c(CH3NH3+)>c(CH3NH2·H2O)> c(H+)>c(OH-),故D错误;故选B。

练习册系列答案
相关题目