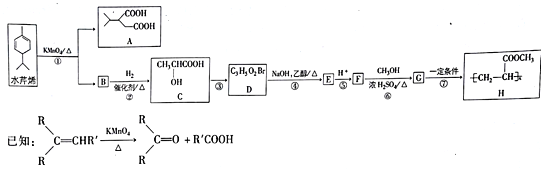
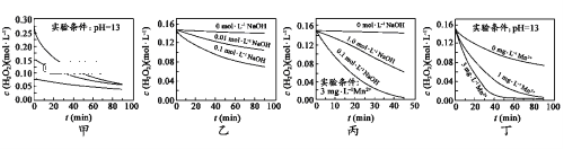
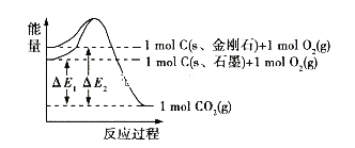
题目内容
【题目】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
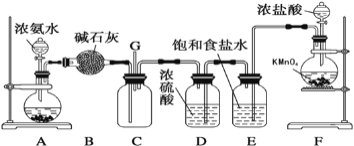
请回答下列问题:
(1)装置F中发生反应的离子方程式为___________________;
(2)盛放浓盐酸的装置的名称是____________;A装置中的固体可能是___________;
(3)通入C装置的两根导管左边较长、右边较短,目的是_____________________;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:___________________________。
【答案】2MnO4-+10Cl-+16H+=Mn2++5Cl2↑+8H2O 分液漏斗 碱石灰或生石灰等 使密度大的氯气与密度小的氨气较快地均匀混合 3Cl2+8NH3=N2+6NH4Cl
【解析】
A装置中产生氨气,通入B的碱石灰干燥后进入C装置;在F中高锰酸钾与浓盐酸反应产生氯气,通过E中饱和食盐水除去氯气中混有的杂质HCl,再通过D装置的浓硫酸对氯气进行干燥,进入C,与氨气混合发生氧化还原反应产生NH4Cl及N2。
(1)装置F中高锰酸钾与浓盐酸反应产生氯气,根据电子守恒、电荷守恒及原子守恒,可得发生反应的离子方程式为2MnO4-+10Cl-+16H+=Mn2++5Cl2↑+8H2O;
(2)根据装置图示可知盛放浓盐酸的装置的名称是分液漏斗;A装置用来制取氨气,A中的固体可能是碱石灰或生石灰、固体NaOH等碱性物质;
(3)通入C装置的两根导管左边较长、右边较短,目的是使密度大的氯气与密度小的氨气较快地均匀混合,以便于充分反应;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,说明氯气与氨气反应生成氯化铵和氮气,根据电子守恒及原子守恒,可得该反应的方程式:3Cl2+8NH3═N2+6NH4Cl。

【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:___________________________;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 15 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=_____,该条件下的平衡常数K=__________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”、“逆向”或“不”);最终达平衡时NO的转化率a=______________。