题目内容
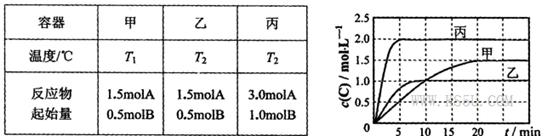
甲、乙、丙三个密闭容器中分别充入一定量的A和B,发生反应: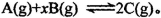 。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:
。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:
下列说法正确的是
A.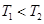 ,且该反应为吸热反应
,且该反应为吸热反应
B.x=2
C.若平衡后保持温度不变,改变容器体积平衡不移动
D.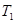 ℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
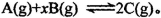 。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:
。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:
下列说法正确的是
A.
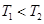 ,且该反应为吸热反应
,且该反应为吸热反应B.x=2
C.若平衡后保持温度不变,改变容器体积平衡不移动
D.
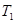 ℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%C
试题分析:A.对于甲、乙来说,起始投入量相同,而反应乙首先达到平衡说明温度T2>T1。在平衡时C(C)(乙) <C(C)(甲),说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理:升高温度,化学平衡向吸热方向移动,逆反应方向是吸热反应,所以正反应是放热反应。错误。B.对乙、丙来说,反应的温度相同,而起始投入量丙是乙的2倍。在其它条件不变的情况下,若增加反应物的浓度,化学平衡不发生移动,则达到化学平衡时C(C)的浓度也应该是乙的2倍。现在2C(C)(乙)=C(C)(丙).说明改变反应物的浓度,化学平衡没有发生改变。只有在反应前后气体体积相等的可逆反应中,改变压强或改变浓度,化学平衡不移动。所以1+X=2,X=1.错误。C. 若平衡后保持温度不变,由于该反应是反应前后气体体积相等的可逆反应。改变容器体积,即改变压强,根据平衡移动原理,化学平衡不移动。正确。D.
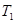 ℃下,起始时向甲容器中充入1.5molA、0.5molB,达到化学平衡时A的转化率为:(0.75÷1.5)×100%=50%.在该温度下,若起始时向甲容器中充入0.5molA、0.5molB,平衡时A的转化率为25%,然后再加入1molB,,增大反应物的浓度,平衡向正反应方向移动,故A的转化率就大于25%。错误。
℃下,起始时向甲容器中充入1.5molA、0.5molB,达到化学平衡时A的转化率为:(0.75÷1.5)×100%=50%.在该温度下,若起始时向甲容器中充入0.5molA、0.5molB,平衡时A的转化率为25%,然后再加入1molB,,增大反应物的浓度,平衡向正反应方向移动,故A的转化率就大于25%。错误。
练习册系列答案
相关题目
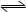 FeO(s)+CO(g)
FeO(s)+CO(g)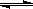 N2O4,下列状态一定是平衡状态的是
N2O4,下列状态一定是平衡状态的是 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 ( )
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 ( ) CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的 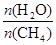 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示: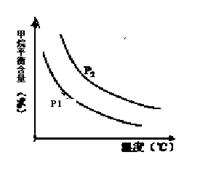
 R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( ) 2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )
2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )