题目内容
下图是制备和研究乙炔的性质实验装置图。下列说法不正确的是

A. 制备乙炔的反应原理是CaC2+2H2O 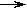 Ca(OH) 2+C2H2↑
Ca(OH) 2+C2H2↑
B. c的作用是除去影响后续实验的杂质
C. d中的有机产物与AgNO3溶液混合能产生沉淀
D. e中的现象说明乙炔能被高锰酸钾酸性溶液氧化
C
【解析】
试题分析:A、制备乙炔用电石与水反应,化学方程式为CaC2+2H2O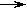 Ca(OH) 2+C2H2↑,正确;B、电石中含S等杂质,所以乙炔气体中含有硫化氢等杂质,硫化氢也能使酸性高锰酸钾溶液褪色,影响实验,必须除去,正确;C、d中的有机产物是溴代烃,溴以原子形式存在,不是离子形式,所以加入硝酸银溶液,不会产生沉淀,错误;D、e中的溶液褪色,说明乙炔能被高锰酸钾酸性溶液氧化,正确,答案选C。
Ca(OH) 2+C2H2↑,正确;B、电石中含S等杂质,所以乙炔气体中含有硫化氢等杂质,硫化氢也能使酸性高锰酸钾溶液褪色,影响实验,必须除去,正确;C、d中的有机产物是溴代烃,溴以原子形式存在,不是离子形式,所以加入硝酸银溶液,不会产生沉淀,错误;D、e中的溶液褪色,说明乙炔能被高锰酸钾酸性溶液氧化,正确,答案选C。
考点:考查实验室制取乙炔的方法及乙炔的化学性质,卤代烃的官能团的检验

(12分)有A、B、C、D、E五种原子序数小于18的元素,其特征信息如下:
元素编号 | 特征信息 |
A | 其中一种原子核内只有质子没有中子 |
B | 其原子的L层电子数是K层的3倍 |
C | 其阳离子与B的阴离子具有相同的电子层结构, 且核电荷数与B相差3 |
D | 其原子的最外层电子数等于电子层数,且是地壳 中含量较多的元素之一 |
E | 单质为黄绿色气体,可用于制造漂白粉 |
请回答以下问题:
(1)由A、B、C三种元素形成的化合物含有的化学键类型是 。
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程
式 。
(3)D单质与由A、B、C三种元素形成的化合物的水溶液反应的离子方程式
。
(4)写出实验室用软锰矿(MnO2)制取E的化学方程式 。
(5)C和D两元素形成的单质活泼些较强的是 (写元素符号),判断依据是 。




