��Ŀ����
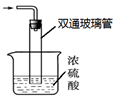
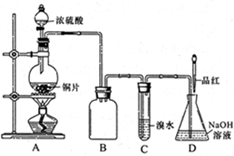
��9�֣����������( Na2S2O3)�����������Լ������ﻹԭ���������ȡ������ֽ⡣��ҵ�Ͽ��÷�Ӧ��2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2�Ƶá�ʵ����ģ��ù�ҵ���̵�װ����ͼ��ʾ��
�ش��������⣺
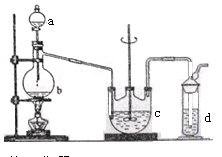
��1��b�з�Ӧ�����ӷ���ʽΪ__________________��c���Լ�Ϊ_____________________��
��2����Ӧ��ʼ��c�����л��Dz��������ֱ���塣�˻�������____________________��
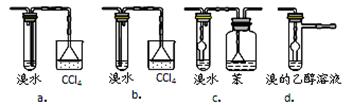
��3��d�е��Լ�Ϊ____________��
��4��ʵ����Ҫ����SO2�������ʣ����Բ�ȡ�Ĵ�ʩ��______________________��д����������
��5��Ϊ�˱�֤��������ƵIJ�����ʵ����ͨ���SO2,���ܹ�����ԭ����_______________________��
�ش��������⣺

��1��b�з�Ӧ�����ӷ���ʽΪ__________________��c���Լ�Ϊ_____________________��
��2����Ӧ��ʼ��c�����л��Dz��������ֱ���塣�˻�������____________________��
��3��d�е��Լ�Ϊ____________��
��4��ʵ����Ҫ����SO2�������ʣ����Բ�ȡ�Ĵ�ʩ��______________________��д����������
��5��Ϊ�˱�֤��������ƵIJ�����ʵ����ͨ���SO2,���ܹ�����ԭ����_______________________��
(1)SO32-+2H+= H2O +SO2��;��HSO3��+H+=SO2��+H2O�����ƺ�̼���ƵĻ����Һ
��2����3��NaOH��Һ ��4�����Ʒ�Ӧ�¶ȡ�������ĵμ��ٶȣ���������Ũ�ȵȣ�
��5����SO2��������Һ�����ԣ�����ֽ�
��2����3��NaOH��Һ ��4�����Ʒ�Ӧ�¶ȡ�������ĵμ��ٶȣ���������Ũ�ȵȣ�
��5����SO2��������Һ�����ԣ�����ֽ�
���������(1)װ��b����ȡSO2��װ�á���b�з�Ӧ�����ӷ���ʽΪSO32-+2H+= H2O +SO2��;��HSO3��+H+=SO2��+H2O�����ݷ�Ӧԭ����֪��c�е��Լ������ƺ�̼���ƵĻ����Һ��(2)��Ӧ��ʼ��c���ȷ�����Ӧ��H2O+SO2+Na2S=H2S+ Na2SO3; SO2+2H2S="3S��+" 2H2O.S�Dz�����ˮ�ĵ���ɫ���ʡ�����л��Dz��������ֱ���壬������Ӧ��2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2��(3) H2S ��SO2���Ǵ�����Ⱦ��������Ƕ����������壬�ܹ�������Ӧ��������d�е��Լ�Ϊǿ��NaOH��Һ��Ϊ��ֹ��������ķ������ڵ����ܵ�ĩ�˰�װ��һ������ܡ�(4)Ӱ�컯ѧ��Ӧ���ʵ����ص�������Ũ�ȡ��¶ȡ��μ��ٶȵȡ���ʵ����Ҫ����SO2�������ʣ����Բ�ȡ�Ĵ�ʩ�п��Ʒ�Ӧ�¶ȡ�������ĵμ��ٶȻ�������Ũ�ȵȡ���5�����������( Na2S2O3)��ǿ�������Σ�������������Ӧ��������SO2��������Һ�����ԣ��������ֽ⡣��˲��ܹ�����

��ϰ��ϵ�д�
�����Ŀ
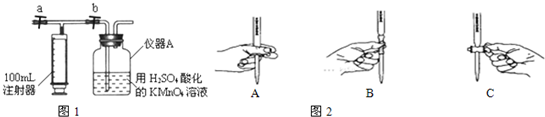
 NH2COONH4(s) ��H��0
NH2COONH4(s) ��H��0