��Ŀ����
һ�������½�2mol SO2��2mol SO3��������һ�̶��ݻ����ܱ������У�������Ӧ��2SO2+O2?2SO3��ƽ��ʱSO3Ϊn mol������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�����ʵ������ܴ���n���ǣ�������
��������ʼͶ��2.0mol SO2�����2.0mol SO3���壬��ЧΪ��ʼͶ��4.0mol SO2�����1mol O2���壬�ں��º����£�ƽ��ʱSO3�����ʵ���Ϊn mol��
����ͬ�¶��£�����������ڸ������з�����ʼ���ʣ���ƽ��ʱ��SO3�����ʵ���������nmol��˵��ƽ�����������ƶ��ˣ��ݴ˽����жϣ�
����ͬ�¶��£�����������ڸ������з�����ʼ���ʣ���ƽ��ʱ��SO3�����ʵ���������nmol��˵��ƽ�����������ƶ��ˣ��ݴ˽����жϣ�
����⣺��ʼͶ��2.0mol SO2�����2.0mol SO3���壬��ЧΪ��ʼͶ��4.0mol SO2�����1mol O2���壬ƽ��ʱSO3�����ʵ���Ϊnmol��
A��2molSO2��1molO2�����ʵ�����4.0mol SO2�����1mol O2�����С��һ�룬�ﵽƽ��ʱ������������ʵ���һ��С��nmol����A����
B��4mol���������1mol��������ԭƽ��Ϊ��ȫ��Чƽ�⣬�ﵽƽ��ʱ��������������ʵ���Ϊnmol����B����
C��2molSO2��1molO2��2molSO3���൱�ڿ�ʼ����4mol��������2mol�������������ʵ�������ѹǿ����ƽ�����������ƶ����ﵽƽ��ʱ������������ʵ�������nmol����C��ȷ��
D��3molSO2��1molO2��1molSO3���൱�ڼ���4mol��������1.5molȥ�������������ʵ�����Ͷ��4.0mol SO2�����1mol O2����Ĵ�ƽ�����������ƶ��������������ʵ���������nmol����D��ȷ��
��ѡ��CD��
A��2molSO2��1molO2�����ʵ�����4.0mol SO2�����1mol O2�����С��һ�룬�ﵽƽ��ʱ������������ʵ���һ��С��nmol����A����
B��4mol���������1mol��������ԭƽ��Ϊ��ȫ��Чƽ�⣬�ﵽƽ��ʱ��������������ʵ���Ϊnmol����B����
C��2molSO2��1molO2��2molSO3���൱�ڿ�ʼ����4mol��������2mol�������������ʵ�������ѹǿ����ƽ�����������ƶ����ﵽƽ��ʱ������������ʵ�������nmol����C��ȷ��
D��3molSO2��1molO2��1molSO3���൱�ڼ���4mol��������1.5molȥ�������������ʵ�����Ͷ��4.0mol SO2�����1mol O2����Ĵ�ƽ�����������ƶ��������������ʵ���������nmol����D��ȷ��
��ѡ��CD��
���������⿼���˿��淴Ӧ��Ҫע���û�ѧƽ���еĵ�Чƽ����жϷ�������ȷ����ת������ʼ���Ĵ�С�ǽ��Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
һ�������½�2mol SO2��2mol SO3��������һ�̶��ݻ����ܱ������У�������Ӧ��2SO2��O2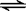 2SO3��ƽ��ʱSO3Ϊn mol������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�����ʵ������ܴ���n����
2SO3��ƽ��ʱSO3Ϊn mol������ͬ�¶��£��ֱ�������������������з�����ʼ���ʣ�ƽ��ʱSO3�����ʵ������ܴ���n����
| A��2 mol SO2�� 1 mol O2 | B��4 mol SO2�� 1 mol O2 |
| C��2 mol SO2�� 1 mol O2�� 2 SO3 | D��3 mol SO2�� 1 SO3 |