题目内容
某科研所欲检测一合金的成分,特做如下实验:取该合金64克,与足量的氯气完全反应,消耗氯气71克,则合金的组成可能是( )
| A、Cu Zn |
| B、Na Zn |
| C、Fe Ca |
| D、Cu Ca |
考点:氯气的化学性质,化学方程式的有关计算
专题:计算题
分析:两种金属组成的合金64克,与足量氯气完全反应,参加反应的氯气为1mol,假设金属都为+2价,则金属的物质的量为1mol,则金属混合物的平衡相对原子质量为64,利用平均值法判断.
解答:
解:两种金属组成的合金64克,与足量氯气完全反应,参加反应的氯气为1mol,设金属都为+2价,金属的物质的量为1mol,则金属混合物的平均相对原子质量为64,
A.Zn的相对原子质量为65,Cu的相对分子质量为64,二者平均相对分子质量介于64~65之间,故A错误;
B.若Na为+2价,则其相对原子质量为46,Zn的相对原子质量为65,二者平均相对分子质量介于46~65之间,故B正确;
C.因为铁与氯气反应生成氯化铁,则Fe为+2价,相对原子质量为56×
=37.4,Ca的相对原子质量为40,二者相对分子质量都小于40,故C错误;
D.Cu的相对分子质量为64,Ca的相对原子质量为40,二者平均相对分子质量介于40~64之间,故D错误;
故选B.
A.Zn的相对原子质量为65,Cu的相对分子质量为64,二者平均相对分子质量介于64~65之间,故A错误;
B.若Na为+2价,则其相对原子质量为46,Zn的相对原子质量为65,二者平均相对分子质量介于46~65之间,故B正确;
C.因为铁与氯气反应生成氯化铁,则Fe为+2价,相对原子质量为56×
| 2 |
| 3 |
D.Cu的相对分子质量为64,Ca的相对原子质量为40,二者平均相对分子质量介于40~64之间,故D错误;
故选B.
点评:本题考查氯气的化学性质及混合物的计算,为高频考点,把握化合价与相对原子质量的转化以及金属在反应中表现的化合价为解答的关键,注意平均值法在该类型题目的应用,题目难度不大.

练习册系列答案
相关题目
苯环上有一个-C4H9和一个-C3H7两个取代基的有机物共有同分异构体( )
| A、12种 | B、4种 |
| C、8种 | D、24种 |
下列关于铯及其化合物的说法中,不正确的( )
| A、氢氧化铯是一种强碱,易溶于水 |
| B、铯与水或酸剧烈反应,都能生成氢气 |
| C、碳酸铯用酒精灯加热可以生成氧化铯和CO2 |
| D、硫酸铯、碳酸铯、硝酸铯都易溶于水 |
下列说法错误的是( )
| A、晶体中有阴离子则必然有阳离子,而有阳离子不一定有阴离子 |
| B、一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| C、原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| D、原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
 如图是某一短周期主族元素最高价氧化物水化物某相同浓度稀溶液与原子半径的关系示意图,则下列说法正确的是( )
如图是某一短周期主族元素最高价氧化物水化物某相同浓度稀溶液与原子半径的关系示意图,则下列说法正确的是( )| A、原子序数:X>Z>W |
| B、气态氢化物的稳定性:N>R |
| C、Y和W形成共价化合物 |
| D、X和Z两者最高价氧化物对应的水化物能相互反应 |
将一小块钠放入CuSO4溶液中,观察到现象是( )
| A、钠溶解,有Cu析出,并有气体产生 |
| B、钠溶解,有蓝色沉淀,有氢气产生 |
| C、有气体产生,无沉淀产生 |
| D、钠在液面逐渐消失,有气体产生和蓝色沉淀 |
25℃、101kPa 下:
①2Na(s)+
O2(g)═Na2O(s)△H1=-414KJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
①2Na(s)+
| 1 |
| 2 |
②2Na(s)+O2(g)═Na2O2(s)△H2=-511KJ/mol
下列说法正确的是( )
| A、①和②产物的阴阳离子个数比相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D、0℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317kJ/mol |
下列过程中能引入卤素原子的是( )
| A、在空气中燃烧 | B、取代反应 |
| C、加成反应 | D、加聚反应 |
某高聚物的结构片段如下:
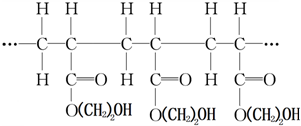
下列分析正确的是( )

下列分析正确的是( )
| A、它是缩聚反应的产物 |
| B、其单体是CH2=CH2COOH和HOCH2CH2OH |
| C、其链节是CH3CH2COO(CH2)2OH |
| D、其单体是CH2=CHCOO(CH2)2OH |