��Ŀ����
����Ŀ��I��ij�¶��£�Kw = 10��12��
��1���������¶Ȳ��䣬������ˮ�м���_________g��NaOH���壬����ˮ��1 L������ʹ��Һ��ˮ���������H+��OH����Ũ�ȳ˻�����c(H+)��c(OH��) = 10��22
��2���������¶Ȳ��䣬ij��Һ��c(H+)Ϊ1��10��7 mol/L�������Һ��________�ԣ�ѡ����������������������������
II����3��ʵ�����г���NaOH����ϴ�����ᴿ����600 mL 1 mol/L NaOH��Һ���ձ�״����8.96 L CO2����ʱ������Һ�и�����Ũ���ɴ�С��˳���� ��
��4����֪������Kw[Fe(OH)3] = 4.0��10��38����FeCl3��Һ�м���NaHCO3��Һ��������Ӧ�����ӷ���ʽΪ_____________������������Һ��pH����Ϊ4������Һ��Fe3+��Ũ��Ϊ__________mol/L��
��5��������ƽ���ƶ�ԭ������������ʵ��FeS������ˮ����������ϡ������_________________��
���𰸡�I����1��4��2����
II����3��c(Na+)>c(HCO3��)>c(CO32��)>c(OH��)>c(H+)
��4��Fe3++3HCO3��=Fe(OH)3��+3CO2�� 4.0��10��8
��5��FeS(s)![]() Fe2+(aq)+S2��(aq)������ϡ�������S2��+2H+=H2S�����ƻ���FeS���ܽ�ƽ����ʹ����ƽ����FeS�ܽ�ķ����ƶ�����FeS�ܽ⡣
Fe2+(aq)+S2��(aq)������ϡ�������S2��+2H+=H2S�����ƻ���FeS���ܽ�ƽ����ʹ����ƽ����FeS�ܽ�ķ����ƶ�����FeS�ܽ⡣
��������
�����������1����ˮ�ĵ��뷽��ʽ��֪��ˮ�������c(H+)����ˮ�������c(OH��)�� �ɵ��������H+��OH����Ũ�ȳ˻� = c(H+)��c(OH��) = 10��22��֪��ˮ�������c(H+) = ˮ�������c(OH��) = 1��10��11 mol/L������NaOH��ǿ�������H2O�Ǽ�������������NaOH�������c(OH��) = c(NaOH) >>ˮ�������c(OH��)������Һ�е�c(OH��) ���Ƶ��� c(NaOH)������Һ����c(H+) = ˮ�������c(H+)����Kw = 10��12 = c(H+)��c(OH��)��c(OH��) = 1��10��1 mol/L����c(NaOH) = 1��10��1 mol/L = 0.1 mol/L����![]() ��ϡ��Һ�����Լ����ˮ�������
��ϡ��Һ�����Լ����ˮ�������![]() ��֪�� c(NaOH) = 0.1 mol/L =
��֪�� c(NaOH) = 0.1 mol/L = 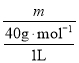 ����m = 4 g����2���������¶Ȳ�����ij��Һ��c(H+)Ϊ1��10��7 mol/L����Kw = 10��12 = c(H+)��c(OH��)��֪��c(OH��) = 1��10��5 mol/L��1��10��5 > 1��10��7������Һ�е�c(H+)С��c(OH��)����˸���Һ�Լ�������3������cV��
����m = 4 g����2���������¶Ȳ�����ij��Һ��c(H+)Ϊ1��10��7 mol/L����Kw = 10��12 = c(H+)��c(OH��)��֪��c(OH��) = 1��10��5 mol/L��1��10��5 > 1��10��7������Һ�е�c(H+)С��c(OH��)����˸���Һ�Լ�������3������cV��![]() ��֪��NaOH��CO2��n�ֱ�Ϊ0.6 mol��0.4mol����NaOH��ϵ��Ϊ6�����⡢ԭ�Ӹ����غ���ƽ�ɵ���6 NaOH + 4 CO2 = 2 Na2CO3 + 2 NaHCO3 + 2 H2O��˵��������Һ��Na2CO3�� NaHCO3��Ũ���������ԼΪ0.33mol/L���������ʶ���ǿ����ʡ�ǿ�������������c(Na+)���������������H2CO3 > HCO3������˶��߶�Ӧ����NaHCO3��Na2CO3����ˮ��̶���HCO3�� < CO32������˴ﵽƽ��ʱ��Һʣ���� c(HCO3��) > c(CO32��)������ˮ��̶Ƚ��������ˮ�����ɵ�c(OH��) < c(CO32��)��ǿ��������ˮ�������ˮ�������������������Һ�������������ƽ��ʱ��Һ��c(H+)��С����4��FeCl3��ǿ����������NaHCO3��ǿ���������������ܷ���˫ˮ�ⷴӦ�������������������Ͷ�����̼����������1����ƽ�ɵ���Fe3+ + 3 HCO3�� = Fe(OH)3�� + 3 CO2��������������Һ��pH����Ϊ4�������Һ�е�c(H+) = 1��10��4 mol/L����������Kw = 10��14 = c(H+)��c(OH��)��c(OH��) = 1��10��10 mol/L����Fe(OH)3
��֪��NaOH��CO2��n�ֱ�Ϊ0.6 mol��0.4mol����NaOH��ϵ��Ϊ6�����⡢ԭ�Ӹ����غ���ƽ�ɵ���6 NaOH + 4 CO2 = 2 Na2CO3 + 2 NaHCO3 + 2 H2O��˵��������Һ��Na2CO3�� NaHCO3��Ũ���������ԼΪ0.33mol/L���������ʶ���ǿ����ʡ�ǿ�������������c(Na+)���������������H2CO3 > HCO3������˶��߶�Ӧ����NaHCO3��Na2CO3����ˮ��̶���HCO3�� < CO32������˴ﵽƽ��ʱ��Һʣ���� c(HCO3��) > c(CO32��)������ˮ��̶Ƚ��������ˮ�����ɵ�c(OH��) < c(CO32��)��ǿ��������ˮ�������ˮ�������������������Һ�������������ƽ��ʱ��Һ��c(H+)��С����4��FeCl3��ǿ����������NaHCO3��ǿ���������������ܷ���˫ˮ�ⷴӦ�������������������Ͷ�����̼����������1����ƽ�ɵ���Fe3+ + 3 HCO3�� = Fe(OH)3�� + 3 CO2��������������Һ��pH����Ϊ4�������Һ�е�c(H+) = 1��10��4 mol/L����������Kw = 10��14 = c(H+)��c(OH��)��c(OH��) = 1��10��10 mol/L����Fe(OH)3 ![]() Fe3+ + 3OH����֪��Kw[Fe(OH)3] = 4.0��10��38 = c(Fe3+) c3(OH��)����c(Fe3+) =
Fe3+ + 3OH����֪��Kw[Fe(OH)3] = 4.0��10��38 = c(Fe3+) c3(OH��)����c(Fe3+) = ![]() mol/L = 4.0��10��8 mol/L����5��FeS(s)
mol/L = 4.0��10��8 mol/L����5��FeS(s)![]() Fe2+(aq) + S2��(aq)������ϡ�������S2�� + 2 H+ = H2S�����ƻ���FeS���ܽ�ƽ����ʹ����ƽ����FeS�ܽ�ķ����ƶ�����FeS������ˮ����������������
Fe2+(aq) + S2��(aq)������ϡ�������S2�� + 2 H+ = H2S�����ƻ���FeS���ܽ�ƽ����ʹ����ƽ����FeS�ܽ�ķ����ƶ�����FeS������ˮ����������������

����Ŀ���ݡ��ο���Ϣ���������п�ѧ�����������21���͵���Դ������δ����ʯ�����Ĺ۵㡣
��1���������������ȼ�յ��Ȼ�ѧ����ʽΪSi��s��+ O2��g���T SiO2��s�� ��H = ��989.2 kJmol��1���йؼ����������±���
��ѧ�� | Si-O | O�TO | Si-Si |
���� / kJmol��1 | x | 498.8 | 176 |
��֪1 mol Si�к�2 mol Si-Si����1 mol SiO2�к�4 mol Si-O������x��ֵΪ__________��
��2���������Ϊһ���ձ�ʹ�õ�������Դ���������ã��������������ص�����˵���У�����Ϊ��������______________��
A����������䡢���棬�Ӱ�ȫ�Ƕȿ��ǣ�������ѵ�ȼ��
B�������Դ�ḻ�����ڿ��ɣ��ҿ�����
C����ȼ�շų�����������ȼ�ղ���Ի�����Ⱦ�̶ȵͣ�������Ч����
D��Ѱ�Ҹ�Ч�´���������ʹ��ӦSiO2 + 2 C![]() Si + 2 CO ���ڳ����·������ǹ���Դ�������õĹؼ�����
Si + 2 CO ���ڳ����·������ǹ���Դ�������õĹؼ�����
��3����ҵ�Ʊ�����ķ�ӦΪ2 H2��g��+ SiCl4��g���T Si��s��+ 4 HCl��g�� ��H = + 240.4 kJmol��1�����ɵ�HClͨ��100 mL 1 molL��1��NaOH��Һǡ����ȫ���������������Ʊ��������Ӧ������__________�����������������ͷ�����������Ϊ__________kJ��
