题目内容
下列关于原子结构、元素性质的说法正确的是( )。
| A.非金属元素组成的化合物中只含共价键 |
| B.ⅠA族金属元素是同周期中金属性最强的元素 |
| C.同种元素的原子均有相同的质子数和中子数 |
| D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
B
解析

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知1~18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同的电子层结构,下列关系正确的是
| A.质子数:c>b | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
有X,Y两种原子,X原子的M电子层比Y原子的M电子层少3个电子,Y原子的L电子层的电子数恰为X原子的L层电子数的2倍,则X,Y元素的元素符号分别为
| A.Mg和S | B.N和Be | C.Si和B | D.C和Al |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是( )
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| C.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是( )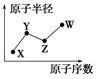
| A.Y、W的最简单氢化物的水溶液都呈酸性 |
| B.X、Y与Z中的任意两种元素均可形成两种或两种以上的化合物 |
| C.上述四种元素形成的化合物都抑制水的电离 |
| D.W的单质可从Z的最简单氢化物中置换出Z的单质 |
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )。
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+与R2-的核外电子数相等
B.M与T形成的化合物既能与酸反应又能与强碱反应
C.氢化物的稳定性为H2T<H2R
D.单质与浓度相等的稀盐酸反应的速率为Q>L
(双选)已知铍(Be)的原子序数为4。下列对铍及其化合物的叙述中,正确的是( )。
| A.铍的原子半径大于硼的原子半径 |
| B.氯化铍难溶于水 |
| C.氢氧化铍的碱性比氢氧化钙的弱 |
| D.单质铍跟冷水反应迅速产生氢气 |
有人建议将氢元素排在元素周期表的第ⅦA族。下列事实能支持这一观点的是( )。
①氢原子得到一个电子后最外层电子达到稳定结构 ②氢分子的结构式为H—H ③与碱金属元素形成离子化合物M+[∶H]- ④分子中原子间的化学键都属于非极性键
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
原子核外的M电子层和L电子层最多容纳的电子数的关系是( )。
| A.大于 | B.小于 | C.等于 | D.不能确定 |