题目内容
(11分)如图所示,已知A元素最低化合价为-3价,它的最高价氧化物含氧56.36%,原子核内中子数比质子数多1个,试回答:
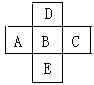
⑴写出它们的元素符号:
A______B______C______D______E______。
⑵A、B、C、D的气态氢化物稳定性最差的是____________。(用分子式表示)写出B的氢化物的结构式____________。
⑶指出C在元素周期表中的位置____________。
⑷A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________。(用分子式表示)

⑴写出它们的元素符号:
A______B______C______D______E______。
⑵A、B、C、D的气态氢化物稳定性最差的是____________。(用分子式表示)写出B的氢化物的结构式____________。
⑶指出C在元素周期表中的位置____________。
⑷A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________。(用分子式表示)
⑴:A :P B :S C:Cl D:O E:S e。
⑵:pH3 ,H-S -H ⑶:第三周期第ⅦA族⑷:HCl O4 >H2S O4 >H3P O4
⑵:pH3 ,H-S -H ⑶:第三周期第ⅦA族⑷:HCl O4 >H2S O4 >H3P O4
(1)A元素最低化合价为-3价,则最高价是+5价,氧化物的化学式为A2O5,所以有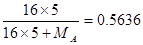 ,解得MA=31。又因为A原子核内中子数比质子数多1个,所以A的质子数是15,即A是磷元素,则B是硫元素,C是氯元素,D是氧元素,E是硒元素。
,解得MA=31。又因为A原子核内中子数比质子数多1个,所以A的质子数是15,即A是磷元素,则B是硫元素,C是氯元素,D是氧元素,E是硒元素。
(2)非金属性越强,相应氢化物的稳定性越强,所以氢化物稳定性最差的是pH3。H2S含有极性键,其结构式为H-S-H。
(3)氯元素位于第三周期第ⅦA族
(4)非金属性越强,最高价氧化物的水化物的酸性越强。非金属性是Cl>S>P,所以HCl O4 >H2S O4 >H3P O4。
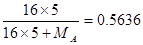 ,解得MA=31。又因为A原子核内中子数比质子数多1个,所以A的质子数是15,即A是磷元素,则B是硫元素,C是氯元素,D是氧元素,E是硒元素。
,解得MA=31。又因为A原子核内中子数比质子数多1个,所以A的质子数是15,即A是磷元素,则B是硫元素,C是氯元素,D是氧元素,E是硒元素。(2)非金属性越强,相应氢化物的稳定性越强,所以氢化物稳定性最差的是pH3。H2S含有极性键,其结构式为H-S-H。
(3)氯元素位于第三周期第ⅦA族
(4)非金属性越强,最高价氧化物的水化物的酸性越强。非金属性是Cl>S>P,所以HCl O4 >H2S O4 >H3P O4。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
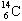 常用于测定动植物标本的年龄。关于
常用于测定动植物标本的年龄。关于