题目内容
【题目】人类生活生产离不开金属,请回答下列问题:
(1)下列现象和事实,不可以用金属活动性做合理解释的是(填序号).①金属镁在空气中比铝更容易燃烧,说明镁比铝的活动性强
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器
④金属的种类很多,但在自然界中,仅有少数金属如金、银等有单质形式存在
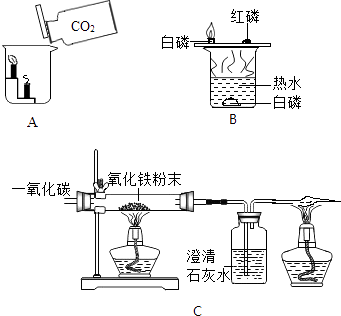
(2)某小组用如图所示装置对铁生锈的条件进行探究,四分钟后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是 . 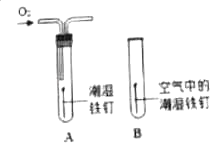
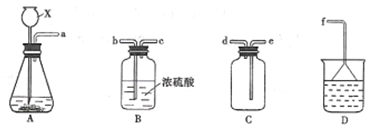
(3)实验室常用10%的稀盐酸除铁锈,再用浓盐酸配置10%稀盐酸的过程中,除了用到烧杯、量筒和胶头滴管外,还需要用到的仪器是 .
(4)请你设计实验验证铜和银的金属活动性顺序,用化学方程式表示为 .
【答案】
(1)②
(2)氧气的浓度
(3)玻璃棒
(4)Cu+2AgNO3═Cu(NO3)2+2Ag
【解析】解:(1)①在相同的条件下,金属与氧气反应时,反应条件越简单,说明该金属的活动性越强;金属镁在空气中比铝更易点燃,说明镁比铝活动性强,故不符合题意;②金属铝更耐腐蚀是由于其化学性质活泼,在常温下就可以和氧气反应而形成致密的氧化铝薄膜,从而阻止进一步氧化,而不是说明锌的活动性比铝强,故符合题意;
③铁的活动性比铜强,所以可以铁能将硫酸铜中的铜置换出来,故不能用铁桶来配制波尔多液,故不符合题意;④自然界中活泼金属以化合物形式存在,活动性弱的金属以单质形式存在,说明了金属的存在形式与金属的活动性有关,故不符合题意.(2)铁生绣的条件是铁与氧气、水共同作用的结果,对比A、B两图,就是空气与氧气的差别,由此可知:氧气的浓度;(3)用浓溶液配制稀溶液时,除了用到烧杯、量筒和胶头滴管外,还需要用到的仪器是玻璃棒.(4)为了验证铜和银的金属活动性顺序,可以将铜丝伸入硝酸银溶液中,铜丝的表面有银生成,化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag.
故答为:(1)②;(2)氧气的浓度;(3)玻璃棒;(4)Cu+2AgNO3═Cu(NO3)2+2Ag.
【考点精析】利用金属活动性顺序及其应用和书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na);注意:a、配平 b、条件 c、箭号.

【题目】利用钻渣[含Co(OH)2、Fe2O3、Al2O3、MnO等)可以来制取钻的氧化物和CoCl2·6H2O,工艺流程如图所示:
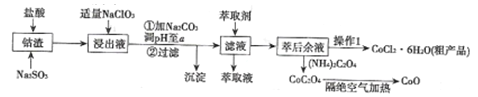
①部分阳离于以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
②CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
回答下列问题:
(1)浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、A13+等,浸出过程中Co(OH)3发生反应的离子方程式为________。
(2)流程中加人适量的NaClO3的作用是___________。若加入NaClO3过量,可能产生有毒气体,写出生成该有毒气体的离子方程式___________________。
(3)加入Na2CO3调节溶液的pH=a,a的范围最好是___________。沉淀的主要成分是______。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。向“滤液”中加入萃取剂的目的是________;其使用的最佳pH范围是________。
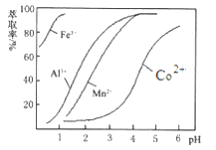
A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(5)“操作1”中包含3个基本实验操作,它们依次是______、______和过滤。
(6)隔绝空气加热CoC2O4生成CoO和碳的氧化物,对应的化学方程式为_______________。